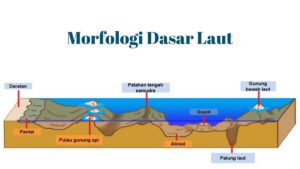
Gugus Amina (NH3+) pada Asam Amino Memiliki Muatan Positif, sebuah fakta kecil yang menjadi penentu besar dalam drama biokimia kehidupan. Bayangkan blok pembangun protein ini bukan sekadar struktur pasif, melainkan entitas dinamis yang membawa muatan listrik, siap berinteraksi dan membentuk kompleksitas makhluk hidup. Pada kondisi netral tubuh kita, gugus amina ini dengan sigap mengikat proton, berubah dari NH2 yang netral menjadi NH3+ yang bermuatan positif, membuka jalan bagi berbagai interaksi kimiawi yang fundamental.
Dalam biokimia, gugus amina (NH3+) pada asam amino membawa muatan positif yang krusial bagi struktur dan fungsi protein. Muatan ini, layaknya dinamika organisasi, dapat menciptakan efek beragam. Seperti halnya Dampak Positif dan Negatif Berdirinya Parpindo , keberadaan muatan positif ini pun punya dua sisi: ia bisa mengikat molekul penting, namun dalam kondisi tertentu justru mengganggu kestabilan. Pada akhirnya, pemahaman atas interaksi muatan positif ini menjadi kunci untuk mengurai kompleksitas sistem biologis yang lebih luas.
Muatan positif ini bukanlah kebetulan, melainkan sifat yang dirancang sempurna oleh alam. Ia menjadi fondasi bagi sifat kelarutan asam amino di dalam air, memungkinkannya beraksi di dalam lingkungan seluler yang cair. Lebih dari itu, muatan inilah yang memungkinkan terjadinya ikatan ionik yang kuat, salah satu kekuatan perekat awal dalam pembentukan struktur protein yang rumit dan fungsional. Keberadaan muatan pada gugus amina menjadikan setiap asam amino bukan hanya penyusun, tetapi juga aktor aktif dalam panggung biologi molekuler.
Pengenalan Gugus Amina Bermuatan pada Asam Amino
Setiap asam amino, sebagai unit pembangun protein, memiliki kerangka dasar yang terdiri dari gugus amina (-NH2), gugus karboksil (-COOH), atom hidrogen, dan rantai samping yang unik. Dalam banyak pembahasan, gugus amina sering digambarkan sebagai -NH2, namun gambaran ini hanya akurat dalam kondisi tertentu. Pada kenyataannya, terutama dalam lingkungan biologis, gugus ini sering kali berada dalam bentuk terprotonasi, yaitu -NH3+, yang membawa muatan positif.
Transformasi dari NH2 menjadi NH3+ ini adalah kunci untuk memahami perilaku asam amino dalam sel hidup.
Status muatan gugus amina sangat bergantung pada pH lingkungannya, sebuah hubungan yang dijelaskan oleh persamaan Henderson-Hasselbalch. Pada pH fisiologis sekitar 7.4, lingkungan di dalam sel kita sedikit basa dibandingkan dengan titik pKa gugus amina alfa (yang umumnya sekitar 9-10). Perbedaan ini menyebabkan gugus amina alfa hampir seluruhnya terprotonasi dan bermuatan positif.
Perbandingan Muatan Gugus Amina pada Berbagai Kondisi pH
Untuk memvisualisasikan pengaruh pH, tabel berikut merangkum keadaan muatan gugus amina alfa dalam berbagai lingkungan kimia.
Dalam biokimia, gugus amina (NH3+) pada asam amino memang bermuatan positif, sebuah prinsip dasar yang mendukung struktur protein. Prinsip dasar seperti ini, yang menopang pengetahuan kita, tidak jauh berbeda dengan cara Penemu Mesin Cetak Ilmuwan Terkenal merevolusi penyebaran ilmu. Revolusi serupa terjadi dalam sains modern, di mana pemahaman mendalam tentang muatan positif gugus amina ini menjadi kunci untuk menguak interaksi molekuler yang kompleks dalam tubuh.
| Kondisi Lingkungan | Perkiraan pH | Status Gugus Amina | Muatan |
|---|---|---|---|
| Lingkungan Asam Kuat | < 2 | Terprotonasi Penuh | +1 (NH3+) |
| Kondisi Fisiologis (Sel) | ~7.4 | Terprotonasi Mayoritas | +1 (NH3+) |
| Pada Titik pKa-nya | ~9-10 | 50% Terprotonasi | +0.5 (Rata-rata) |
| Lingkungan Basa Kuat | > 12 | Terprotonasi Minimal | 0 (NH2) |
Muatan positif pada gugus NH3+ ini bukan sekadar detail kimiawi. Muatan ini bersifat krusial karena menjadi fondasi bagi sifat amfoter asam amino, memungkinkan mereka bertindak sebagai buffer alami. Lebih penting lagi, muatan ini memfasilitasi berbagai interaksi elektrostatik yang menentukan struktur tiga dimensi protein, fungsi enzimatik, dan kemampuan molekul ini untuk larut dalam medium berair seperti sitosol sel.
Sifat Kimia dan Interaksi Gugus NH3+: Gugus Amina (NH3+) Pada Asam Amino Memiliki Muatan Positif
Kehadiran muatan positif pada gugus amina membuka pintu bagi beragam interaksi kimia yang elegan dan fundamental. Interaksi ini menjadi bahasa yang digunakan oleh asam amino dan protein untuk membentuk struktur kompleks dan menjalankan fungsinya dengan presisi.
Ikatan Ionik dan Jembatan Garam
Gugus NH3+ dengan muatan positifnya secara alami tertarik kepada gugus yang bermuatan negatif. Interaksi elektrostatik yang kuat ini, sering disebut ikatan ionik, adalah salah satu kekuatan pengatur dalam arsitektur protein. Interaksi spesifik antara gugus NH3+ dari satu residu asam amino dengan gugus karboksilat (COO-) dari residu lain dikenal sebagai jembatan garam (salt bridge). Jembatan garam berperan sebagai paku molekuler yang menstabilkan lipatan protein tertentu, terutama pada struktur tersier dan kuaterner.
Contoh klasik dapat ditemukan pada enzim lisozim. Pada molekul ini, jembatan garam terbentuk antara gugus NH3+ pada residu lisin (Lys) ke-1 dengan gugus COO- pada residu asam glutamat (Glu) ke-7. Interaksi ini membantu menstabilkan struktur tiga dimensi enzim yang penting untuk fungsinya dalam memecah dinding sel bakteri.
Pengaruh terhadap Kelarutan dalam Air
Muatan positif pada gugus NH3+, bersama dengan muatan negatif dari gugus karboksilat yang terdeprotonasi (COO-), menjadikan asam amino dalam bentuk zwitterion sangat polar. Molekul air, yang juga polar, dapat berinteraksi kuat dengan kedua muatan ini melalui ikatan hidrogen dan solvasi ionik. Interaksi yang kuat ini membuat asam amino umumnya sangat larut dalam air, sebuah sifat esensial bagi semua proses biokimia yang terjadi dalam medium akuatik di dalam sel.
Peran Biologis dan Implikasinya
Melampaui sifat kimia dasarnya, muatan positif pada gugus amina memainkan peran langsung dan tak tergantikan dalam mekanisme kehidupan. Dari menyambung molekul hingga mengenali substrat, NH3+ adalah pemain kunci di panggung seluler.
Pembentukan Ikatan Peptida, Gugus Amina (NH3+) pada Asam Amino Memiliki Muatan Positif
Proses sintesis protein dimulai dengan penyatuan asam amino melalui ikatan peptida. Reaksi kondensasi ini digerakkan oleh nukleofil, yaitu pasangan elektron bebas pada nitrogen gugus amina (dari asam amino kedua) yang menyerang gugus karbonil karboksil (dari asam amino pertama). Pada pH fisiologis, nitrogen ini adalah bagian dari NH3+, namun proton dari nitrogen ini akan dilepaskan selama dan setelah reaksi untuk membentuk ikatan peptida yang baru.
Dengan demikian, sifat nukleofilik dari nitrogen amina, yang dipengaruhi oleh lingkungan muatannya, adalah prasyarat untuk pembentukan tulang punggung protein.
Fungsi pada Situs Aktif dan Pengikatan
Banyak asam amino dengan rantai samping yang juga mengandung gugus amina bermuatan positif, seperti lisin dan arginin, sering ditemukan di situs aktif enzim atau wilayah pengikatan protein. Muatan positif mereka digunakan untuk berinteraksi dengan substrat, kofaktor, atau molekul lain yang mengandung gugus bermuatan negatif, seperti gugus fosfat pada ATP atau molekul DNA. Interaksi ini memastikan pengikatan yang spesifik dan orientasi yang tepat untuk katalisis atau regulasi.
Perbandingan Peran Gugus NH3+ pada Beberapa Asam Amino Spesifik
Tidak semua gugus amina bermuatan positif diciptakan sama. Lokasi dan sifat kimiawinya yang sedikit berbeda memberikan peran yang unik bagi masing-masing asam amino.
| Asam Amino | Gugus Bermuatan Positif | Nilai pKa Rantai Samping | Peran Biologis Utama |
|---|---|---|---|
| Lisin (Lys, K) | -NH3+ pada ujung rantai samping | ~10.5 | Stabilisasi struktur via jembatan garam, modifikasi kimia (asetilasi, metilasi), pengikatan ligan negatif. |
| Arginin (Arg, R) | Guanidinium (-C(NH2)2+) | ~12.5 | Interaksi yang sangat kuat dengan gugus fosfat (misal, pada DNA), sering pada situs pengikatan. |
| Histidin (His, H) | Imidazolium (pada cincin imidazol) | ~6.0 | Bertindak sebagai donor/akseptor proton pada pH fisiologis; krusial dalam katalisis enzimatik (misal, pada enzim protease serine). |
Kontekstualisasi dalam Sistem yang Lebih Kompleks
Pengaruh gugus NH3+ menjadi semakin menarik dan kompleks ketika kita melihat skala yang lebih besar, yaitu pada level protein utuh dan dalam dinamika modifikasi seluler. Di sini, muatan positif kolektif menjadi alat yang digunakan sel untuk mengatur nasib dan fungsi molekul proteinnya.
Muatan Total dan Titik Isoelektrik (pI) Protein
Setiap protein terdiri dari banyak asam amino, masing-masing menyumbang muatannya pada pH tertentu. Jumlah aljabar dari semua muatan positif (dari gugus NH3+ alfa dan rantai samping lisin, arginin) dan muatan negatif (dari gugus COO- dan rantai samping asam aspartat, glutamat) menghasilkan muatan total protein. Titik isoelektrik (pI) adalah pH spesifik di mana muatan total ini menjadi nol. Nilai pI ini menentukan perilaku protein dalam medan listrik (seperti pada elektroforesis) dan kelarutannya; protein cenderung mengendap pada pH mendekati pI-nya.
Dengan demikian, kontribusi setiap gugus NH3+ membantu menentukan identitas elektrokimia keseluruhan protein.
Peran sebagai Buffer Biologis
Kemampuan gugus amina, terutama yang ada pada rantai samping histidin dengan pKa-nya yang unik (~6.0), untuk menerima atau mendonorkan proton menjadikannya komponen buffer yang sangat efektif dalam rentang pH fisiologis. Dengan bertindak sebagai “spons proton,” gugus-gugus ini membantu menstabilkan pH internal sel dan organel terhadap fluktuasi yang disebabkan oleh aktivitas metabolik, sehingga menjaga lingkungan yang optimal bagi fungsi enzim dan proses seluler lainnya.
Modifikasi Pasca-Translasi dan Netralisasi Muatan
Fungsi protein dapat diatur secara dinamis melalui modifikasi pasca-translasi. Salah satu modifikasi umum pada residu lisin adalah asetilasi, diimana gugus asetil (-COCH3) ditambahkan ke nitrogen gugus NH3+, mengubahnya menjadi -NHCOCH3 yang netral. Netralisasi muatan positif ini dapat secara drastis mengubah interaksi elektrostatik protein, mempengaruhi lipatannya, stabilitas, atau kemampuan berikatan dengan DNA atau protein lain. Modifikasi ini adalah mekanisme epigenetik kunci dalam regulasi ekspresi gen melalui modifikasi histon.
Ilustrasi dan Visualisasi Konseptual
Memahami konsep molekuler seringkali terbantu dengan gambaran mental yang jelas. Berikut adalah deskripsi tekstual untuk membantu memvisualisasikan konsep-konsep kunci terkait gugus NH3+.
Visualisasi Molekul Lisin dengan Distribusi Muatan
Bayangkan struktur molekul lisin pada pH fisiologis. Di tengah, terdapat atom karbon alfa (Cα) yang mengikat empat gugus berbeda. Di satu sisi, terdapat gugus karboksilat (COO-) yang bermuatan negatif, terdeprotonasi. Di sisi berlawanan, terdapat gugus amina alfa (NH3+) yang bermuatan positif, terprotonasi. Yang membedakan lisin adalah rantai sampingnya yang panjang dan fleksibel, yang pada ujungnya juga terdapat gugus amina primer (NH3+) lain yang bermuatan positif.
Jadi, molekul lisin digambarkan dengan dua “bola” bermuatan positif (satu di bagian tengah/alfa dan satu di ujung rantai) dan satu “bola” bermuatan negatif, dihubungkan oleh rangka hidrokarbon. Distribusi muatan ini membuatnya sangat polar dan reaktif secara elektrostatik.
Gugus amina (NH3+) pada asam amino memang membawa muatan positif, sebuah konsep elektrokimia yang fundamental dalam biologi. Prinsip muatan dan gaya ini ternyata punya analogi menarik dengan dunia fisika, misalnya saat menganalisis tekanan dalam zat cair melalui Soal dan Jawaban Fisika Fluida Statis. Pemahaman tentang gaya dan keseimbangan fluida itu membantu kita membayangkan bagaimana interaksi elektrostatik dari gugus NH3+ yang bermuatan positif dapat memengaruhi struktur dan fungsi protein dalam medium cair.
Bagan Alur Perubahan Muatan Gugus Amina terhadap pH
Source: slidesharecdn.com
Sebuah bagan alur sederhana dapat menggambarkan transisi ini: Pada sumbu horizontal adalah pH, dari rendah (asam) ke tinggi (basa). Sebuah kurva dimulai di bagian atas grafik, menandakan populasi spesies NH3+ yang mendekati 100%. Kurva ini tetap tinggi dan datar seiring kenaikan pH. Ketika pH mendekati nilai pKa gugus amina (sekitar 9-10), kurva mulai turun dengan tajam membentuk bentuk sigmoid. Pada titik pKa, kurva berada tepat di tengah (50% NH3+, 50% NH2).
Setelah melewati pKa, kurva terus turun hingga mendekati nol, menandakan populasi spesies NH2 yang mendominasi pada pH basa kuat. Garis vertikal pada pH 7.4 akan memotong kurva di bagian atas yang masih datar, mengonfirmasi bahwa pada kondisi sel, gugus amina hampir seluruhnya bermuatan positif.
Interaksi Gugus NH3+ dengan DNA dalam Kompleks Protein-Nukleat
Visualisasikan sebuah heliks ganda DNA, dengan tulang punggung gula-fosfatnya yang berulang menampilkan deretan gugus fosfat bermuatan negatif. Sekarang, bayangkan sebuah protein pengikat DNA, seperti faktor transkripsi, mendekati alur utama DNA. Pada permukaan protein yang menghadap DNA, terdapat beberapa residu lisin dan arginin yang menonjol keluar. Gugus NH3+ pada lisin dan gugus guanidinium pada arginin, dengan muatan positifnya, secara elektrostatik tertarik dan berbaris sempurna dengan gugus fosfat negatif pada tulang punggung DNA.
Interaksi multipel ini, seperti rangkaian magnet kecil, mengikat protein dengan erat dan spesifik pada urutan DNA tertentu, memungkinkan protein untuk membaca dan mengatur informasi genetik.
Ringkasan Penutup
Dari pembahasan mendalam ini, menjadi jelas bahwa muatan positif pada gugus amina (NH3+) jauh lebih dari sekadar detail kimiawi. Ia adalah karakter penentu yang mengalir dari sifat dasar asam amino hingga fungsi rumit protein dalam sel. Interaksi elektrostatik yang dimungkinkan oleh muatan ini menjadi bahasa universal untuk membentuk struktur, mengatalisis reaksi, dan meregulasi proses kehidupan. Pemahaman akan peran sentral NH3+ ini membuka jendela untuk mengapresiasi keanggunan dan presisi desain molekuler di balik setiap makhluk hidup, sekaligus landasan kokoh bagi pengembangan terapi dan bioteknologi masa depan.
FAQ dan Panduan
Apakah muatan positif pada gugus amina selalu permanen?
Tidak. Muatan pada gugus NH3+ sangat bergantung pada pH lingkungan. Pada kondisi sangat basa (pH tinggi), gugus ini dapat kehilangan protonnya dan kembali menjadi NH2 yang netral.
Bagaimana muatan positif ini mempengaruhi cara obat bekerja di dalam tubuh?
Banyak obat dirancang untuk meniru atau berinteraksi dengan gugus bermuatan pada asam amino. Muatan positif pada NH3+ dapat digunakan untuk menargetkan bagian protein tertentu yang bermuatan negatif, meningkatkan spesifisitas dan efektivitas obat.
Apakah semua asam amino memiliki gugus amina (NH3+) yang bermuatan positif pada kondisi yang sama?
Secara umum, ya, gugus amina alfa (yang terikat pada atom karbon pusat) hampir selalu terprotonasi (NH3+) pada pH fisiologis. Namun, asam amino seperti lisin dan arginin memiliki rantai samping dengan gugus amina tambahan yang juga bermuatan positif, sehingga memberikan muatan total yang lebih besar.
Dapatkah muatan positif pada gugus amina menyebabkan masalah dalam sel?
Ya, jika tidak diregulasi. Muatan berlebih dapat mengganggu pelipatan protein atau menyebabkan agregasi yang tidak diinginkan. Karena itulah, sel memiliki mekanisme seperti modifikasi pasca-translasi (misalnya asetilasi) untuk menetralkan muatan positif tertentu saat diperlukan.