Penggunaan Logam Mg sebagai Pelindung Katodik untuk Logam Fe adalah sebuah solusi cerdas nan elegan yang diambil dari prinsip dasar alam. Bayangkan, logam yang lebih aktif seperti magnesium dengan sukarela “mengorbankan” dirinya untuk melindungi besi dari kerusakan karat yang menggerogoti. Teknik ini bukan sekadar teori di laboratorium, melainkan sudah diaplikasikan dalam kehidupan sehari-hari, dari tangki air panas di rumah hingga pipa baja yang terkubur jauh di dalam tanah.
Prinsipnya sederhana namun sangat efektif, mengubah kelemahan korosi menjadi sebuah mekanisme pertahanan yang terencana.
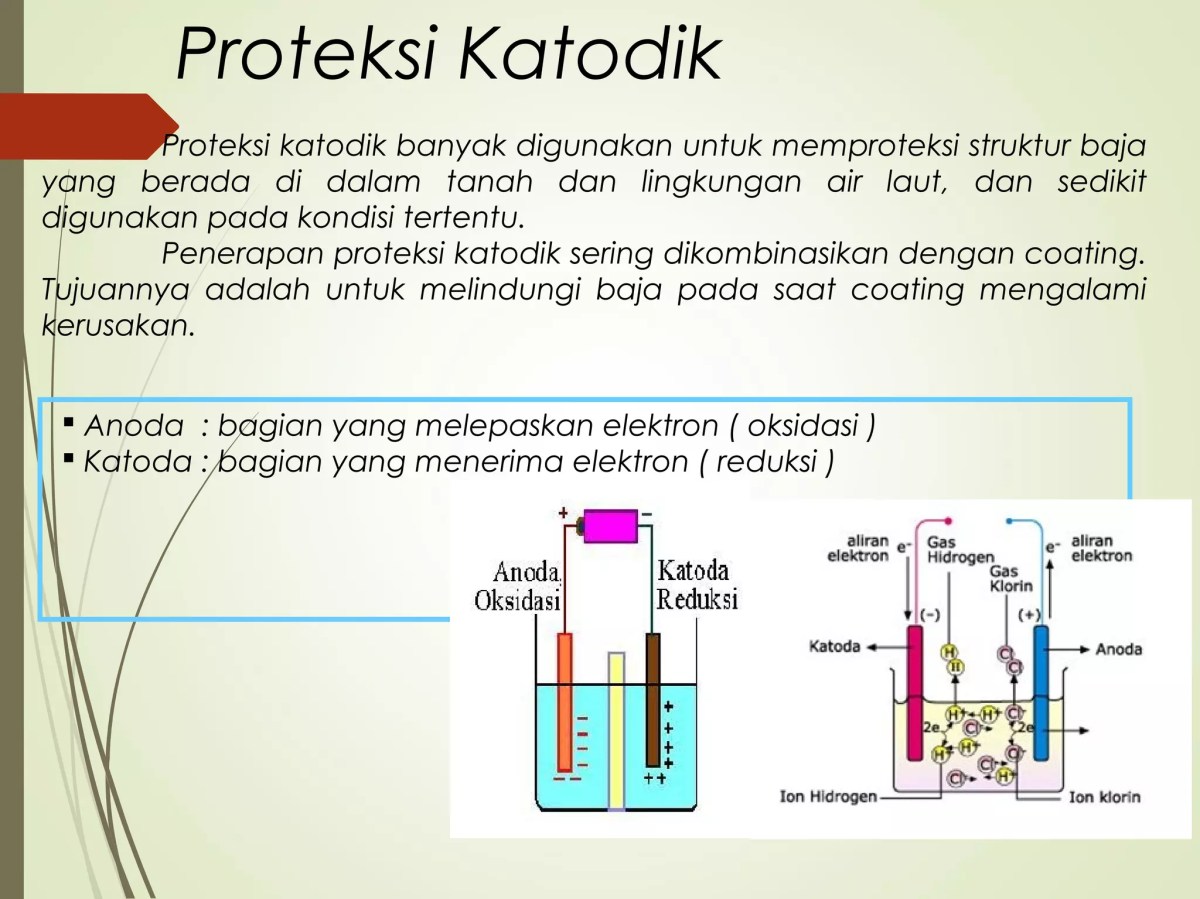
Pada dasarnya, perlindungan katodik bekerja dengan memanfaatkan deret elektrokimia, di mana magnesium yang lebih reaktif akan teroksidasi lebih dulu dibandingkan besi. Ketika kedua logam ini terhubung dalam lingkungan elektrolit seperti air atau tanah lembap, terbentuklah sel galvanik mikro. Arus listrik mengalir dari magnesium (anoda) ke besi (katoda), sehingga seluruh permukaan besi menjadi terkathodisasi dan proses koronsinya terhenti. Metode ini menjadi pilihan utama karena sifatnya yang pasif, tidak memerlukan sumber listrik eksternal, dan memberikan proteksi yang merata pada struktur yang kompleks.
Dalam dunia korosi, penggunaan logam Mg sebagai pelindung katodik untuk logam Fe merupakan strategi cerdas yang memanfaatkan potensial elektroda lebih negatif magnesium. Prinsip ini mengingatkan kita pada pentingnya struktur kalimat yang tepat untuk menyampaikan ide, sebagaimana dibahas dalam artikel Mengisi titik pada kalimat My father … tea dan menjelaskan tenses yang mengurai presisi penggunaan tenses. Demikian halnya dalam proteksi katodik, ketepatan pemilihan material pelindung dan pemahaman mekanisme reaksi redoks menjadi kunci utama efektivitasnya dalam mencegah karat pada besi.
Dasar-dasar Korosi dan Perlindungan Katodik
Korosi pada besi, terutama karat yang kita kenal sehari-hari, bukanlah sekadar proses kimia biasa. Ia adalah sebuah reaksi elektrokimia yang teratur. Dalam lingkungan yang mengandung elektrolit—seperti air, tanah lembap, atau udara lembap—permukaan besi bertindak seperti sel elektrokimia mini. Area tertentu bertindak sebagai anoda, di mana besi teroksidasi melepaskan elektron (Fe → Fe²⁺ + 2e⁻). Elektron-elektron ini kemudian mengalir di dalam logam menuju area katoda, di mana mereka dikonsumsi oleh reaksi reduksi, biasanya reduksi oksigen (O₂ + 2H₂O + 4e⁻ → 4OH⁻).
Aliran elektron inilah yang menjadi inti dari kerusakan logam.
Prinsip perlindungan katodik justru memanfaatkan mekanisme alami korosi ini, namun dengan mengalihkan “korban”-nya. Jika dalam korosi galvanik dua logam berbeda yang kurang ajar bersentuhan menyebabkan logam yang lebih aktif (kurang mulia) terkikis, maka dalam perlindungan katodik, kita sengaja memasangkan logam yang jauh lebih aktif—seperti magnesium—dengan besi. Tujuannya adalah memaksa seluruh permukaan besi menjadi katoda, sehingga reaksi oksidasi (pelepasan material) hanya terjadi pada logam pelindung tersebut.
Magnesium (Mg) adalah pilihan yang sangat tepat sebagai “anoda korban” untuk melindungi besi (Fe). Alasan utamanya terletak pada sifat elektrokimianya yang sangat kuat. Dalam deret elektrokimia, magnesium menempati posisi yang jauh lebih aktif (lebih mudah teroksidasi) dibandingkan besi. Perbedaan potensial yang besar ini menciptakan “gaya dorong” atau arus perlindungan yang kuat, cukup untuk melindungi area besi yang luas. Selain itu, magnesium memiliki kapasitas arus teoritis yang tinggi, artinya setiap kilogram magnesium dapat menyediakan jumlah elektron yang besar untuk perlindungan dalam jangka waktu tertentu.
Dalam dunia teknik material, prinsip perlindungan katodik menggunakan logam Mg untuk Fe mengandalkan perhitungan elektrokimia yang presisi. Konsep perhitungan sistematis ini juga vital di ranah pendidikan, misalnya saat Menghitung Jumlah Mahasiswa Lulus Berdasarkan Distribusi Nilai Ujian Matematika , yang memerlukan analisis data akurat. Demikian halnya, efektivitas proteksi Mg pada baja sangat ditentukan oleh ketepatan kalkulasi laju korosi dan potensial elektrode untuk memastikan keberhasilan aplikasinya.
Perbandingan Metode Pencegahan Korosi
Selain perlindungan katodik, terdapat beberapa metode lain yang umum digunakan. Memahami perbedaan mendasar antar metode ini membantu dalam menentukan strategi proteksi yang paling efektif dan ekonomis untuk suatu aplikasi.
| Metode | Prinsip Kerja | Kelebihan Utama | Keterbatasan |
|---|---|---|---|
| Perlindungan Katodik (Anoda Mg) | Mengorbankan logam aktif (Mg) untuk melindungi besi dengan menjadikannya katoda. | Proteksi menyeluruh, efektif untuk struktur kompleks dan tersembunyi, perawatan relatif sederhana. | Umur anoda terbatas dan perlu diganti, efektivitas bergantung pada kondisi lingkungan (resistivitas tanah/air). |
| Pelapisan (Cat, Epoxy, Galvanisasi) | Membentuk lapisan fisik yang menghalangi kontak besi dengan lingkungan korosif. | Biaya awal sering lebih rendah, memberikan perlindungan sekaligus estetika. | Proteksi hilang jika lapisan rusak/terkelupas (korosi dimulai dari titik cacat), memerlukan surface preparation yang baik. |
| Inhibitor Korosi | Menambahkan senyawa kimia ke lingkungan (seperti dalam coolant radiator) untuk menekan reaksi elektrokimia. | Praktis untuk sistem tertutup/bercirculasi seperti pipa, mesin, dan radiator. | Hanya efektif pada lingkungan dengan konsentrasi inhibitor yang terjaga, perlu monitoring dan replenishment, berpotensi polusi. |
| Material Tahan Korosi (Stainless Steel) | Mengganti material besi karbon dengan paduan yang membentuk lapisan pasif oksida pelindung. | Daya tahan sangat tinggi, umur panjang, sering tidak memerlukan proteksi tambahan. | Biaya material dan fabrikasi jauh lebih tinggi, tidak praktis untuk struktur besar yang sudah ada. |
Sifat dan Reaktivitas Logam Magnesium: Penggunaan Logam Mg Sebagai Pelindung Katodik Untuk Logam Fe
Kecocokan magnesium sebagai penjaga besi tidak datang begitu saja. Ia dibekali dengan serangkaian sifat fisika dan kimia yang unik. Secara fisika, magnesium adalah logam yang ringan (densitas ~1.74 g/cm³), memiliki konduktivitas listrik dan panas yang baik, serta relatif mudah difabrikasi. Sifat ringan ini menjadi nilai tambah dalam aplikasi di mana beban menjadi pertimbangan, seperti pada kapal.
Dalam dunia material, prinsip perlindungan katodik menggunakan logam Mg untuk Fe mengandalkan sifat elektrokimia yang lebih aktif. Fenomena perubahan material akibat interaksi dengan lingkungan juga terjadi pada tekstil, misalnya bagaimana Serat Hewan Menjadi Lebih Halus Saat Sering Dicuci. Sama halnya, proses korosi pada Fe dan penghalusan serat adalah transformasi bertahap. Kembali ke konteks teknik, pengorbanan Mg sebagai anode justru menjadi kunci efektivitas proteksi jangka panjang bagi struktur besi.
Namun, kunci utamanya ada pada sifat kimia dan elektrokimianya. Dalam deret elektrokimia (seri galvanik), magnesium adalah salah satu logam struktural yang paling aktif. Potensial elektrodanya yang sangat negatif, sekitar -2.37 V terhadap elektrode hidrogen standar, menempatkannya jauh di atas besi (-0.44 V). Perbedaan potensial yang mencapai hampir 2 volt ini adalah “mesin” yang menggerakkan sistem proteksi. Posisinya yang sangat aktif berarti magnesium memiliki kecenderungan yang sangat kuat untuk melepaskan elektron, sehingga dengan mudah “mengambil alih” peran sebagai anoda dalam sel korosi, menyelamatkan besi dari proses oksidasi.
Reaksi Elektrokimia pada Sistem Mg-Fe
Ketika magnesium terhubung secara elektrik dengan besi dan keduanya terendam dalam elektrolit yang sama, sebuah sirkuit listrik lengkap terbentuk. Pada anoda magnesium, terjadi reaksi oksidasi yang tak terhindarkan:
Mg → Mg²⁺ + 2e⁻
Elektron-elektron yang dilepaskan ini kemudian mengalir melalui koneksi logam (kabel atau kontak langsung) menuju permukaan besi. Di permukaan besi yang kini berperan sebagai katoda, elektron-elektron tersebut dikonsumsi oleh reaksi reduksi. Reaksi reduksi yang paling umum dalam lingkungan netral atau basa (seperti air atau tanah) adalah reduksi oksigen terlarut:
O₂ + 2H₂O + 4e⁻ → 4OH⁻
Ion Mg²⁺ yang terbentuk akan bereaksi dengan ion OH⁻ dari katoda, membentuk magnesium hidroksida (Mg(OH)₂) yang mengendap sebagai produk korosi putih. Reaksi keseluruhan ini secara efektif menghentikan pembentukan ion Fe²⁺, sehingga besi terlindungi.
Reaktivitas tinggi magnesium ini adalah pedang bermata dua. Di satu sisi, ia memberikan daya proteksi yang kuat. Di sisi lain, ia menuntut penanganan yang hati-hati.
Dalam aplikasi tangki air panas domestik, reaktivitas magnesium memastikan proteksi maksimal terhadap badan tangki besi. Namun, di air dengan resistivitas sangat rendah (sangat konduktif) atau suhu tinggi, reaksi bisa berlangsung terlalu cepat. Anoda mungkin habis sebelum waktunya, atau justru menghasilkan arus berlebih yang menyebabkan pengendapan berlebihan dan potensi penyumbatan. Selain itu, dalam kondisi tertentu, produk korosi magnesium yang berlebihan dapat mempengaruhi kualitas air, memberikan rasa atau kekeruhan tertentu.
Mekanisme Perlindungan Katodik Menggunakan Mg
Proses perlindungan dimulai seketika sistem terpasang dan terpapar elektrolit. Bayangkan sebuah pipa besi yang dikubur di tanah lembab, dengan batang magnesium yang dihubungkan padanya. Tanah bertindak sebagai elektrolit. Ion-ion dalam kelembaban tanah memungkinkan arus listrik mengalir. Segera setelah terhubung, perbedaan potensial alami antara Mg dan Fe mendorong elektron mengalir dari Mg (melalui kabel) menuju Fe.
Aliran elektron ini adalah arus perlindungan.
Arus ini kemudian menyebar dari titik sambungan ke seluruh permukaan pipa besi. Distribusinya tidak selalu merata; area yang dekat dengan anoda magnesium cenderung menerima kerapatan arus yang lebih tinggi dibandingkan area yang jauh. Namun, jika jumlah dan penempatan anoda tepat, seluruh permukaan besi akan mencapai potensial yang cukup negatif (biasanya lebih negatif dari -0.85 V terhadap elektrode tembaga/tembaga sulfat) untuk menghentikan korosi sama sekali.
Perubahan potensial ini adalah tanda bahwa besi telah sepenuhnya menjadi katoda.
Faktor yang Mempengaruhi Efektivitas Anoda Mg
Efektivitas dan kecepatan konsumsi anoda magnesium tidak mutlak. Beberapa faktor kunci yang mengaturnya antara lain:
- Resistivitas Lingkungan: Tanah atau air dengan resistivitas tinggi (konduktivitas rendah) akan membatasi aliran arus, mengurangi jangkauan proteksi dan memperlambat konsumsi anoda. Sebaliknya, lingkungan dengan resistivitas sangat rendah (air laut) akan mempercepat konsumsi.
- Perbedaan Potensial dan Polarisasi: Potensial awal Mg yang sangat negatif dapat mengalami polarisasi (berkurang) karena terbentuknya lapisan produk korosi di permukaannya, yang dapat sedikit mengurangi daya dorong arus.
- Rasio Area: Rasio antara luas permukaan anoda magnesium dan luas permukaan besi yang dilindungi. Area proteksi yang terlalu luas untuk satu anoda akan mengurangi kerapatan arus dan menurunkan level proteksi.
- Kualitas Sambungan Elektrik: Sambungan yang buruk, berkarat, atau longgar akan meningkatkan resistansi, menghambat aliran arus proteksi dan membuat sistem tidak efektif.
Prosedur Pemasangan Anoda Magnesium
Source: slidesharecdn.com
Pemasangan yang benar sangat menentukan kinerja sistem. Untuk struktur terendam (seperti tangki), anoda Mg biasanya diulirkan langsung ke dinding tangki atau digantung dengan kabel dan diisolasi agar tidak jatuh. Sambungan kabel harus bersih, kencang, dan dilindungi dari korosi. Untuk struktur yang dikubur (seperti pipa), anoda Mg ditempatkan di dalam backfill khusus (biasanya campuran gipsum, bentonit, dan natrium sulfat) yang berfungsi menurunkan resistansi tanah di sekitar anoda, menjaga kelembaban, dan melarutkan produk korosi.
Anoda harus diletakkan pada kedalaman yang cukup dan posisi yang strategis untuk distribusi arus optimal. Dalam wadah tertutup seperti pemanas air, anoda langsung dipasang pada flensa atau lubang yang disediakan, memastikan kontak logam yang baik dengan badan tangki.
Aplikasi dan Bentuk Anoda Magnesium dalam Praktik
Di pasaran, anoda magnesium hadir dalam berbagai bentuk untuk menyesuaikan dengan kebutuhan aplikasi yang beragam. Bentuk yang paling umum adalah batang silinder (rod) dengan inti kabel baja yang sudah tertanam, yang mudah dipasang pada tangki atau struktur. Untuk proteksi eksternal pipa panjang atau dasar kapal, tersedia anoda bentuk pita (ribbon) yang dapat dililitkan atau dipasang sepanjang struktur. Ada juga bentuk khusus seperti plug, wafer, atau bentuk yang dirancang khusus untuk wadah tertentu.
Dalam kehidupan sehari-hari, penerapannya sering kita temui tanpa disadari. Anoda batang magnesium adalah komponen standar di dalam pemanas air listrik (water heater) untuk melindungi tabung baja dari korosi akibat air panas. Pada kapal kecil atau perahu fiberglass dengan motor tempel, anoda magnesium sering dipasang di unit kemudi atau lambung untuk melindungi baut, poros baling-baling, dan komponen logam lainnya dari korosi galvanik di air tawar.
Untuk pipa bawah tanah dari baja, anoda magnesium dalam backfill dipasang pada interval tertentu sepanjang jalur pipa.
Spesifikasi Bentuk Anoda Magnesium
| Bentuk | Spesifikasi Umum | Kelebihan | Batasan |
|---|---|---|---|
| Batang (Rod) dengan Kabel | Diameter 1-3 inci, panjang 15-60 cm, dengan kabel tembaga inti baja. | Pemasangan mudah (diulir/digantung), cocok untuk tangki, boiler, dan wadah tertutup. | Jangkauan proteksi terbatas pada area di sekitarnya, bentuk kurang fleksibel. |
| Pita (Ribbon) | Penampang persegi panjang, panjang bisa puluhan meter, fleksibel. | Dapat melindungi area linier panjang (pipa), distribusi arus lebih merata sepanjang jalur. | Pemasangan lebih rumit, memerlukan isolasi dan penempatan yang hati-hati di tanah. |
| Bentuk Khusus (Plug, Wafer) | Disesuaikan dengan flange atau lubang standar pada peralatan. | Integrasi sempurna dengan desain peralatan, penggantian sangat mudah. | Hanya cocok untuk aplikasi spesifik yang telah dirancang sebelumnya. |
Pertimbangan Kemurnian versus Paduan
Magnesium untuk anoda korban tidak selalu murni 100%. Pilihan antara magnesium murni (Grade M1) dan paduan (seperti Mg-Al-Zn-Mn) bergantung pada kondisi lingkungan. Magnesium murni memiliki potensial yang paling negatif, cocok untuk lingkungan dengan resistivitas tinggi seperti air tawar atau tanah kering. Namun, ia cenderung membentuk lapisan film yang dapat menyebabkan polarisasi berlebihan. Paduan magnesium, meski potensialnya sedikit kurang negatif, sering kali memiliki efisiensi arus yang lebih baik (persentase material yang benar-benar digunakan untuk menghasilkan arus proteksi lebih tinggi) dan produk korosinya lebih mudah rontok, sehingga cocok untuk lingkungan dengan resistivitas lebih rendah atau yang membutuhkan performa lebih konsisten.
Kelebihan, Kekurangan, dan Pemeliharaan Sistem
Menggunakan magnesium sebagai anoda korban menawarkan sejumlah keunggulan dibandingkan material lain seperti seng atau aluminium. Kelebihan utamanya adalah potensial penggeraknya yang sangat besar, memungkinkan proteksi yang andal bahkan di lingkungan dengan resistivitas relatif tinggi di mana seng atau aluminium mungkin tidak efektif. Magnesium juga relatif aman digunakan di air tawar tanpa risiko pembentukan lapisan pasif yang berlebihan yang dapat menghentikan proteksi.
Dari sisi biaya awal, sistem magnesium biasanya lebih murah untuk diaplikasikan dibandingkan sistem proteksi katodik arus paksa (impressed current) yang memerlukan rectifier dan anoda inert.
Namun, sistem ini bukan tanpa cacat. Kekurangan utama adalah umur pakainya yang terbatas dan perlu penggantian berkala. Konsumsi magnesium bisa sangat cepat di lingkungan yang sangat konduktif seperti air laut, sehingga kurang ekonomis. Terdapat juga risiko “over-protection” jika arus yang dihasilkan terlalu besar untuk struktur besi tertentu, terutama pada baja kekuatan tinggi, yang dapat menyebabkan keretakan akibat hidrogen. Produk korosi magnesium hidroksida yang berlebihan dapat menimbulkan endapan dan, dalam sistem air tertutup, mempengaruhi kualitas air.
Panduan Inspeksi dan Penggantian
Pemeliharaan sistem anoda magnesium bersifat preventif dan terencana. Inspeksi visual dan pengukuran potensial harus dilakukan secara berkala, biasanya setiap 1-2 tahun. Anoda yang telah habis akan terlihat menyusut secara signifikan, sering kali hanya menyisakan inti kabel baja. Pengukuran potensial struktur terhadap elektrode referensi akan menunjukkan jika nilai proteksi telah turun di bawah level aman (kurang negatif dari -0.85 V CSE).
Penggantian harus dilakukan sebelum anoda benar-benar habis. Prosedurnya sederhana: matikan atau isolasi sistem jika memungkinkan, lepaskan sambungan kabel anoda lama, pasang anoda baru dengan sambungan yang bersih dan kencang, dan pastikan kontak listriknya baik.
Pengaruh Kondisi Lingkungan
Kinerja anoda magnesium sangat dipengaruhi oleh lingkungan sekitarnya. pH rendah (lingkungan asam) akan mempercepat konsumsi magnesium secara drastis. Resistivitas tanah atau air adalah faktor penentu utama; semakin rendah resistivitas, semakin besar arus yang bisa dihasilkan dan semakin cepat anoda habis. Suhu tinggi juga mempercepat semua reaksi kimia, termasuk korosi pada anoda. Oleh karena itu, desain sistem—seperti jumlah, ukuran, dan penempatan anoda—harus didasarkan pada karakteristik lingkungan spesifik lokasi pemasangan untuk mencapai umur pakai dan efektivitas yang diinginkan.
Studi Kasus dan Analisis Performa
Mari kita rancang sebuah skenario aplikasi nyata: sebuah tangki penyimpanan air bersih dari baja karbon, berdiameter 3 meter dan tinggi 5 meter (luas permukaan interior sekitar 60 m²), beroperasi di lingkungan air tawar dengan suhu ambient. Untuk melindunginya, dipasang dua buah anoda magnesium batang, masing-masing berat 7 kg. Dengan asumsi efisiensi arus magnesium 50% dan kebutuhan kerapatan arus proteksi 10 mA/m² untuk air tengar, kita dapat mengestimasi umur anoda.
Kapasitas teoritis magnesium adalah sekitar 2200 Ah/kg. Dengan efisiensi 50%, kapasitas efektif menjadi 1100 Ah/kg. Total kapasitas untuk dua anoda (14 kg) adalah 14 kg
– 1100 Ah/kg = 15,400 Ah. Kebutuhan arus total untuk melindungi 60 m² adalah 60 m²
– 0.01 A/m² = 0.6 A. Maka, estimasi umur anoda = Total Kapasitas (Ah) / Arus (A) = 15,400 Ah / 0.6 A = 25,667 jam, atau sekitar 2.9 tahun.
Dalam praktik, umur ini bisa sedikit berbeda tergantung fluktuasi kualitas air dan suhu.
Analisis Data Potensial dan Standar Proteksi, Penggunaan Logam Mg sebagai Pelindung Katodik untuk Logam Fe
Setelah pemasangan, pengukuran potensial pada berbagai titik dinding tangki terhadap elektrode Cu/CuSO4 menunjukkan pembacaan yang konsisten antara -1.05 V hingga -0.95 V. Nilai-nilai ini berada jauh di bawah batas kritis -0.85 V yang ditetapkan oleh standar seperti NACE SP0169 atau ISO 15589-1 untuk proteksi katodik pada baja dalam lingkungan tanah atau air. Ini mengindikasikan bahwa seluruh permukaan tangki menerima proteksi yang memadai.
Polarisasi minimal 100 mV dari potensial korosi alami besi juga tercapai, yang merupakan kriteria proteksi lainnya.
Perbandingan Efektivitas Biaya Jangka Panjang
Untuk tangki dengan skala ini, mari bandingkan tiga opsi: (1) Sistem anoda magnesium (seperti studi kasus), (2) Pelapisan internal epoxy berkualitas tinggi, dan (3) Sistem proteksi katodik arus paksa (ICCP). Biaya awal termurah adalah pelapisan, diikuti anoda Mg, dan yang tertinggi adalah ICCP. Namun, dalam jangka 15 tahun, pelapisan mungkin memerlukan touch-up atau pelapisan ulang jika ada kerusakan. Anoda Mg memerlukan penggantian setiap ~3 tahun dengan biaya material dan tenaga yang rendah.
ICCP memiliki biaya operasi listrik yang sangat rendah dan umur anoda inert yang panjang. Analisis siklus hidup sering menunjukkan bahwa untuk aplikasi tangki air sederhana, sistem anoda magnesium menawarkan keseimbangan terbaik antara biaya awal, kemudahan pemeliharaan, dan keandalan proteksi tanpa ketergantungan pada listrik.
Faktor Kritis Keberhasilan Aplikasi
- Desain yang Tepat: Perhitungan jumlah, ukuran, dan penempatan anoda berdasarkan luas area, kondisi lingkungan, dan umur desain yang diinginkan.
- Kualitas Material dan Pemasangan: Penggunaan anoda dengan spesifikasi sesuai, sambungan listrik yang bersih dan kokoh, serta pemasangan yang mengikuti prosedur.
- Monitoring Berkala: Pengukuran potensial proteksi secara rutin untuk memastikan sistem masih berfungsi optimal dan menentukan waktu penggantian anoda secara proaktif.
- Pemahaman Lingkungan: Karakterisasi awal kondisi air atau tanah (resistivitas, pH, suhu) sebagai dasar desain yang akurat.
- Integritas Lapisan (jika ada): Pada struktur yang juga dilapisi, menjaga lapisan dalam kondisi baik akan sangat mengurangi kebutuhan arus proteksi, sehingga memperpanjang umur anoda magnesium secara signifikan.
Terakhir
Dari pembahasan mendalam dapat disimpulkan bahwa magnesium memang merupakan pilihan yang sangat strategis sebagai anoda korban untuk melindungi besi. Efektivitasnya yang tinggi, kemudahan aplikasi, dan biaya yang relatif terjangkau menjadikannya solusi yang populer di berbagai sektor. Meski memiliki tantangan seperti laju konsumsi yang perlu dipantau dan pembentukan produk korosi, perhitungan yang matang dan pemeliharaan rutin dapat mengoptimalkan kinerjanya. Pada akhirnya, inovasi sederhana ini membuktikan bahwa memahami hukum alam dan menerapkannya dengan tepat adalah kunci untuk melawan degradasi material, memperpanjang usia pakai infrastruktur, dan menghemat biaya dalam jangka panjang.
FAQ Terperinci
Apakah anoda magnesium bisa digunakan untuk melindungi logam selain besi?
Ya, prinsipnya bisa selama logam yang dilindungi (katoda) lebih mulia dalam deret elektrokimia dibandingkan magnesium. Namun, aplikasi paling umum dan efektif adalah untuk melindungi baja (besi) dan baja berlapis seng.
Bagaimana cara mengetahui kapan anoda magnesium harus diganti?
Anoda magnesium harus diganti ketika massanya telah berkurang signifikan (biasanya 60-70% habis) atau ketika pengukuran potensial proteksi pada struktur besi sudah tidak memenuhi standar lagi. Inspeksi visual berkala sangat dianjurkan.
Apakah ada risiko bahaya dari penggunaan magnesium sebagai anoda korban?
Risiko utamanya adalah pembentukan gas hidrogen selama reaksi korosi, yang dapat terkumpul di ruang tertutup dan berpotensi meledak jika ada sumber percikan. Selain itu, produk korosi magnesium yang berlebihan dapat menyumbat sistem.
Bisakah anoda magnesium bekerja efektif di air tawar?
Ya, bisa. Namun efektivitas dan laju konsumsinya sangat dipengaruhi oleh resistivitas air. Air tawar dengan resistivitas tinggi (seperti air murni) akan memperlambat laju proteksi, sehingga mungkin memerlukan lebih banyak atau bentuk anoda yang berbeda dibandingkan di air laut.

