Rumus Struktur dan Senyawa Hidrokarbon 3‑Etil‑2,2‑Dimetilpentana itu seperti puzzle karbon yang bikin penasaran. Kalau cuma dengar namanya yang panjang, bisa-bisa langsung bikin mata berkunang-kunang. Tapi percayalah, di balik deretan kata itu tersimpan cerita menarik tentang bagaimana atom-atom berorganisasi, membentuk struktur unik yang punya karakter sendiri. Mari kita bongkar bareng-bareng, biar yang terlihat rumit jadi seru untuk dipelajari.
Senyawa ini sebenarnya adalah alkana rantai bercabang dengan sembilan atom karbon. Namanya yang sistematis, 3-Etil-2,2-Dimetilpentana, sudah langsung menyebarkan petunjuk tentang susunannya: rantai utama pentana (5 karbon) yang dihiasi oleh gugus etil dan dua gugus metil di posisi spesifik. Dari sini, kita bisa mulai melacak jejak atom karbon dan hidrogennya, lalu menggambarkan kerangkanya, yang ternyata punya bentuk tiga dimensi yang cukup nge-gas untuk dibayangkan.
Pengenalan dan Identifikasi Dasar Senyawa
Nama senyawa kimia seringkali terdengar seperti mantra ajaib, tapi sebenarnya ia adalah petunjuk lengkap yang menceritakan struktur molekulnya. Mari kita bongkar nama “3-Etil-2,2-Dimetilpentana” kata per kata. “Pentana” adalah jantung dari senyawa ini, menandakan rantai karbon lurus utama yang terdiri dari 5 atom karbon (pent-). Kemudian, ada dua jenis tamu yang menempel di rantai utama itu: sebuah gugus “etil” (dua atom karbon, -C₂H₅) yang terikat pada atom karbon nomor 3, dan dua gugus “metil” (satu atom karbon, -CH₃) yang keduanya terikat pada atom karbon nomor 2.
Awalan “di-” pada dimetil memberitahu kita bahwa ada dua gugus metil di posisi yang sama.
Gugus Alkil dan Komposisi Atom
Dari namanya, kita bisa mengidentifikasi semua gugus alkil yang terikat. Pada atom karbon nomor 2 dari rantai pentana, terikat dua gugus metil. Pada atom karbon nomor 3, terikat satu gugus etil. Untuk menghitung total atom, kita mulai dari rantai utama pentana (C5) lalu tambahkan: dua metil memberi tambahan 2 atom C, dan satu etil memberi tambahan 2 atom C. Total atom karbon adalah 5 + 2 + 2 = 9 atom C (C9).
Setiap atom karbon memiliki ikatan yang harus terpenuhi. Setelah menghitung semua ikatan, jumlah atom hidrogen yang menyertainya adalah 20. Jadi, secara keseluruhan, molekul ini dibangun dari 9 atom karbon dan 20 atom hidrogen.
Penulisan dan Analisis Rumus Struktur
Setelah mengetahui komposisinya, langkah selanjutnya adalah menuangkannya ke dalam bentuk rumus, baik itu rumus molekul yang sederhana maupun gambar struktur yang lebih kaya informasi. Ini adalah cara kita memvisualisasikan molekul di atas kertas sebelum membayangkannya dalam ruang tiga dimensi.
Rumus Molekul dan Struktur Rajut
Rumus molekul dari senyawa ini adalah C9H
20. Untuk menggambar rumus struktur rajut (kerangka), ikuti langkah-langkah sistematis ini:
- Gambarlah rantai utama pentana sebagai garis zig-zag dengan 5 titik sudut (masing-masing mewakili atom C). Beri nomor dari 1 sampai 5.
- Pada atom karbon nomor 2 (titik sudut kedua), gambarlah dua garis cabang pendek yang keluar dari titik yang sama. Ini mewakili dua gugus metil (-CH3).
- Pada atom karbon nomor 3 (titik sudut ketiga), gambarlah satu garis cabang yang lebih panjang. Di ujung garis ini, buat titik baru. Ini adalah gugus etil (-CH2-CH3), yang berarti dari atom C nomor 3, terikat sebuah CH2 yang kemudian terikat lagi dengan CH3.
- Pastikan semua atom karbon (setiap ujung garis dan titik sudut) memiliki empat ikatan. Atom hidrogen tidak digambar dalam rumus rajut, mereka dianggap mengisi sisa ikatan yang tersisa.
Struktur yang bercabang ini menghasilkan beberapa jenis atom karbon berdasarkan jumlah atom karbon lain yang terikat padanya.
| Jenis Atom Karbon | Deskripsi (Jumlah ikatan ke C lain) | Contoh dalam Struktur | Jumlah |
|---|---|---|---|
| Primer (1°) | Terikat pada 1 atom C lain | Ujung rantai (C1, C5), ujung gugus etil, ujung metil | 6 |
| Sekunder (2°) | Terikat pada 2 atom C lain | C4 pada rantai utama | 1 |
| Tersier (3°) | Terikat pada 3 atom C lain | C3 pada rantai utama (terikat ke C2, C4, dan gugus etil) | 1 |
| Kuarterner (4°) | Terikat pada 4 atom C lain | C2 pada rantai utama (terikat ke C1, C3, dan dua metil) | 1 |
Tata Nama IUPAC dan Isomer
Tata nama IUPAC bukan sekadar aturan, melainkan bahasa universal yang memastikan setiap struktur memiliki satu nama yang unik dan jelas. Proses pemberian nama adalah kebalikan dari membaca nama. Kita memilih rantai terpanjang, memberi nomor yang memberikan lokasi cabang dengan angka terkecil, dan menyusun nama secara alfabetis.
Proses Penamaan dan Isomer Rantai, Rumus Struktur dan Senyawa Hidrokarbon 3‑Etil‑2,2‑Dimetilpentana
Jika diberikan struktur 3-Etil-2,2-Dimetilpentana, proses penamaan IUPAC-nya akan mengonfirmasi nama tersebut. Rantai karbon terpanjang adalah pentana (5 C). Penomoran dimulai dari ujung yang memberikan angka terkecil untuk posisi cabang. Dari ujung kiri, cabang ada di posisi 2 dan 3. Dari ujung kanan, cabang akan ada di posisi 3 dan 4.
Karena 2,3 lebih kecil dari 3,4, penomoran yang benar adalah dari ujung kiri. Cabangnya adalah dua metil di C2 dan satu etil di C3. Nama disusun secara alfabetis (etil sebelum metil), dengan awalan “di-” untuk metil, menjadi 3-Etil-2,2-Dimetilpentana.
Mari kita lihat struktur 3-Etil-2,2-Dimetilpentana. Senyawa hidrokarbon ini punya rantai utama pentana dengan cabang etil dan dua gugus metil yang tertata rapi di posisi spesifik, mirip seperti bagaimana sebuah kelompok sosial butuh Kerja Sama Terencana dalam Kelompok Sosial untuk mencapai tujuan bersama. Nah, dalam kimia, presisi penempatan gugus fungsi ini krusial—sama halnya presisi dalam berkolaborasi—agar rumus struktur akhirnya stabil dan berfungsi sempurna.
Senyawa ini memiliki rumus molekul C9H20, yang sama dengan semua nonana. Namun, karena strukturnya bercabang, ia bukan nonana lurus, melainkan salah satu dari banyak isomer rantai nonana.
- 3-Etil-2,2-Dimetilpentana memiliki rantai utama hanya 5 karbon dengan percabangan yang padat di tengah, menghasilkan bentuk yang lebih kompak dan globular.
- Nonana lurus (n-nonana) memiliki rantai karbon panjang berkelok tanpa cabang.
- Isomer-isomer lain, seperti 2,2,4,4-Tetrametilpentana, memiliki titik percabangan dan rantai utama yang berbeda, meski jumlah atom C dan H-nya persis sama.
Penomoran rantai utama selalu dimulai dari ujung yang memberikan angka terkecil (atau seri angka terkecil) untuk posisi cabang. Ini adalah aturan emas IUPAC untuk memastikan keseragaman. Pada senyawa ini, memulai dari ujung yang salah akan memberi nomor 3 dan 4 pada cabang, yang secara numerik lebih besar dari 2 dan 3.
Sifat Fisik dan Kimia yang Relevan
Struktur molekul tidak hanya sekadar gambar; ia adalah penentu sifat. Bagaimana sebuah molekul berinteraksi dengan sesamanya atau dengan pelarut sangat bergantung pada bentuk dan percabangannya. Percabangan pada 3-Etil-2,2-Dimetilpentana memberinya karakteristik yang menarik dibandingkan dengan alkana lurus.
Pengaruh Percabangan pada Sifat Fisik
Dibandingkan dengan n-nonana (nonana lurus), 3-Etil-2,2-Dimetilpentana diperkirakan memiliki titik didih yang lebih rendah. Alasannya adalah bentuk molekulnya yang bercabang dan seperti bola mengurangi luas permukaan kontak antar molekul. Gaya antarmolekul (gaya London) pada alkana sangat bergantung pada luas permukaan ini. Molekul yang lebih kompak tidak bisa saling mendekat dan berinteraksi seefektif molekul lurus yang panjang, sehingga energi yang dibutuhkan untuk memisahkan mereka (titik didih) lebih rendah.
Senyawa ini juga akan sangat larut dalam pelarut non-polar seperti heksana atau CCl4, mengikuti prinsip “like dissolves like”, karena ia sendiri adalah molekul non-polar yang murni.
Keberadaan dua gugus metil pada satu atom karbon (C2 kuarterner) menciptakan struktur yang sangat stabil secara sterik. Cabang-cabang ini justru “melindungi” pusat yang padat tersebut. Namun, secara keseluruhan, percabangan mengurangi kerapatan molekul karena menghalangi pengepakan yang rapat dalam fase cair, yang juga berkontribusi pada titik didih yang lebih rendah.
Dalam keluarga alkana, semakin tinggi tingkat percabangan, titik didih isomer akan semakin rendah dibandingkan isomer rantai lurusnya. Contoh: n-nonana mendidih di sekitar 151°C, sedangkan 3-Etil-2,2-Dimetilpentana dan isomer bercabang lainnya akan mendidih pada suhu yang lebih rendah, seringkali dalam rentang 140-145°C, karena bentuk molekulnya yang lebih bulat.
Visualisasi 3D dan Konformasi Molekul
Membayangkan molekul dalam ruang tiga dimensi adalah kunci untuk memahami perilakunya yang sebenarnya. Bayangkan kita memegang model ball-and-stick: bola untuk atom, stik untuk ikatan. Dari sini, kita bisa membahas bentuk, sudut, dan kemungkinan gerakannya.
Deskripsi Model 3D dan Konformasi
Dalam model ball-and-stick 3D, molekul 3-Etil-2,2-Dimetilpentana akan terlihat seperti huruf “T” yang tebal dan tidak simetris. Rantai utama pentana membentuk dasar huruf “T” yang miring. Pada atom karbon nomor 2 (pusat dari palang atas “T”), dua gugus metil akan menjorok ke arah yang berlawanan, membentuk sudut ikatan kira-kira 109.5° khas tetrahedral. Gugus etil yang terikat pada C3 akan memanjang ke arah samping, menambah kesan volume yang padat di bagian tengah molekul.
Orientasi ini meminimalkan tolakan antar gugus alkil yang besar.
Rantai pentana utamanya dapat berotasi di sekitar ikatan tunggal C-C, mengadopsi berbagai konformasi seperti
-anti* atau
-gauche*. Namun, keberadaan cabang etil dan dua metil yang besar menimbulkan halangan sterik yang signifikan. Rotasi tertentu, terutama di sekitar ikatan C2-C3, akan sangat terhambat karena gugus-gugus besar ini akan saling bertabrakan. Hal ini membatasi jumlah konformasi yang benar-benar stabil dan nyaman bagi molekul ini, membuatnya cenderung memilih konformasi di mana cabang-cabang tersebut saling menjauh sebisa mungkin.
Kemungkinan Isomer Optik dan Geometri
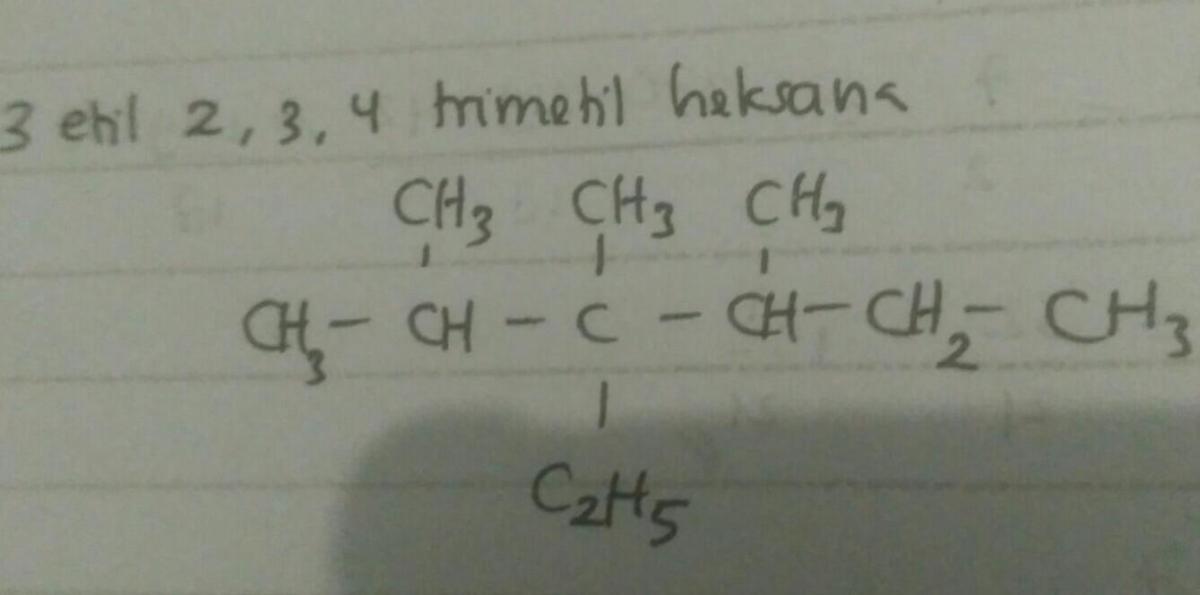
Source: z-dn.net
Untuk memiliki isomer optik (kiral), sebuah molekul harus memiliki atom karbon kiral, yaitu atom karbon yang terikat pada empat gugus yang berbeda. Mari kita periksa atom karbon dalam struktur ini. Atom C2 adalah kuarterner dan terikat pada dua gugus metil yang identik, sehingga tidak kiral. Atom C3 adalah tersier, tetapi ia terikat pada: sebuah H (dari asumsi struktur alkana), sebuah -CH2- dari rantai utama (menuju C4), sebuah -CH2- dari gugus etil, dan sebuah cabang yang berisi C1 dan dua metil di C2.
Mempelajari rumus struktur 3-Etil-2,2-dimetilpentana itu seperti mengurai puzzle atom karbon; ada kepuasan tersendiri saat kita berhasil memvisualisasikan rantainya. Nah, dalam refleksi, fokus pada hal-hal teknis yang kurang substansial justru bisa mengaburkan makna, mirip seperti saat kita terjebak pada Hal yang Tidak Penting Saat Merefleksi Isi Puisi. Jadi, kembali ke senyawa hidrokarbon tadi, intinya adalah memahami pola ikatannya, bukan sekadar menghafal nama yang panjang itu.
Meski kompleks, dua dari empat “lengan” tersebut (rantai ke C4 dan gugus etil) tidak identik, tetapi lengan yang keempat (cabang yang mengandung C1 dan dua metil di C2) adalah unik. Namun, untuk menjadikan C3 kiral, keempat gugus harus benar-benar berbeda. Analisis mendetail menunjukkan bahwa tidak ada atom karbon dalam molekul ini yang terikat pada empat gugus yang
-semuanya* berbeda satu sama lain.
Selain itu, karena tidak ada ikatan rangkap yang kaku, isomer geometri (*cis-trans*) juga tidak mungkin terjadi pada alkana jenuh ini. Jadi, senyawa 3-Etil-2,2-Dimetilpentana tidak memiliki isomer optik maupun geometri; ia adalah molekul akiral.
Ringkasan Akhir: Rumus Struktur Dan Senyawa Hidrokarbon 3‑Etil‑2,2‑Dimetilpentana
Jadi, begitulah perjalanan mengulik 3-Etil-2,2-Dimetilpentana. Dari sekadar nama IUPAC yang panjang, kita berhasil membedahnya jadi rumus struktur, menganalisis jenis atom karbonnya, sampai memprediksi sifat fisiknya. Senyawa ini adalah contoh sempurna betapa percabangan bisa mengubah sifat sebuah molekul, menurunkan titik didih, dan memberi bentuk yang lebih kompak. Pemahaman ini nggak cuma teori belaka, tapi fondasi untuk menjelajah dunia kimia organik yang lebih luas dan menakjubkan.
Bagian Pertanyaan Umum (FAQ)
Apakah 3-Etil-2,2-Dimetilpentana bisa ditemukan di alam atau hanya dibuat di lab?
Senyawa ini termasuk alkana sintetis dan lebih banyak dibuat di laboratorium untuk keperluan studi. Meski alkana umum ditemukan di minyak bumi, isomer bercabang spesifik seperti ini biasanya tidak melimpah secara alami.
Bagaimana cara cepat membedakan senyawa ini dari isomer C9H20 lainnya hanya dari namanya?
Perhatikan angka dan awalan di namanya. “2,2-Dimetil” menunjukkan ada dua cabang metil di atom karbon nomor 2 yang sama, sebuah pola percabangan yang khas. Isomer lain seperti nonana (rantai lurus) atau 4-etilheptana akan memiliki pola penomoran dan cabang yang berbeda.
Apakah senyawa ini berbahaya atau mudah terbakar?
Sebagai alkana, senyawa ini kemungkinan mudah terbakar seperti hidrokarbon lain, tetapi data spesifik mengenai toksisitas dan bahayanya perlu merujuk pada lembar data keselamatan material (MSDS) karena sangat bergantung pada kemurnian dan bentuk fisiknya.
Mengapa tidak ada isomer optik atau geometri pada senyawa ini?
Senyawa ini tidak memiliki isomer optik karena tidak ada atom karbon kiral (yang mengikat empat gugus berbeda) dalam strukturnya. Juga, tidak ada isomer geometri karena semua ikatan karbon-karbon pada alkana ini adalah ikatan tunggal yang bebas berotasi.


