Antibiotik Spesifik untuk Typhus: Inhibisi Enzim Peptidoglycan bukan sekadar judul riset yang rumit, melainkan pintu gerbang menuju era baru penanganan demam tifoid yang lebih tepat sasaran. Bayangkan, alih-alih membombardir semua bakteri dengan antibiotik spektrum luas, kita kini bisa mengirim ‘pasukan khusus’ yang secara cerdas melumpuhkan musuh tepat di pusat pertahanannya. Strategi ini berfokus pada enzim peptidoglycan, komponen krusial yang menjadi tulang punggung dinding sel bakteri Salmonella typhi.
Dengan menghambat enzim spesifik ini, sintesis dinding sel terhenti dan bakteri pun kolaps. Pendekatan yang presisi ini menjanjikan efektivitas tinggi dengan dampak samping yang lebih minimal, karena tidak mengganggu mikroflora baik dalam tubuh. Inilah terobosan yang mengubah paradigma, dari terapi yang bersifat umum menuju serangan yang ditujukan tepat pada sasaran molekuler si patogen penyebab typhus.
Peran Enzim Peptidoglycan dan Dasar Ilmiah Penghambatannya
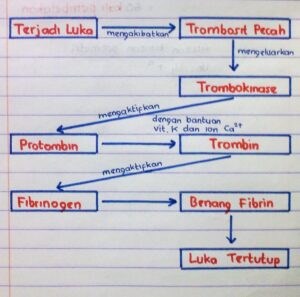
Dinding sel bakteri, khususnya pada Salmonella typhi, bukan sekadar pelindung pasif. Ia adalah struktur dinamis yang terus diperbarui dan diperluas seiring pertumbuhan dan pembelahan bakteri. Komponen utamanya adalah peptidoglycan, sebuah jaring raksasa yang terbuat dari rantai gula dan peptida yang saling menyilang, memberikan kekuatan mekanik dan menjaga integritas sel. Sintesis lapisan kaku ini melibatkan serangkaian enzim yang bekerja seperti jalur perakitan nan presisi.
Enzim-enzim seperti transglycosylase dan transpeptidase memegang peran kunci. Transglycosylase bertugas merangkai rantai gula (glycan) yang panjang, sementara transpeptidase bertindak sebagai “tukang las”, menghubungkan rantai peptida yang berdekatan untuk membentuk jaring silang yang kuat. Tanpa aktivitas enzim-enzim ini, bakteri tidak dapat membangun dinding sel baru. Sel yang mencoba membelah akan menjadi rapuh dan akhirnya lisis atau pecah karena tekanan osmotik internalnya sendiri.
Mekanisme Dasar Inhibisi Enzim Peptidoglycan
Antibiotik yang menargetkan enzim peptidoglycan bekerja dengan prinsip sabotase molekuler. Mereka dirancang untuk meniru struktur substrat alami enzim—baik itu molekul gula maupun peptida—namun dengan pengaturan atom yang membuatnya tidak dapat diproses lebih lanjut. Ketika antibiotik ini masuk ke situs aktif enzim, ia akan terikat dengan erat, menghalangi substrat asli untuk masuk. Enzim pun menjadi mandek, terhambat, atau malah mengikat senyawa palsu yang kemudian mengacaukan seluruh proses perakitan.
Hasil akhirnya adalah cacat fatal pada dinding sel. Bakteri yang sedang aktif berkembang biak akan menghasilkan dinding sel yang penuh lubang, lemah, dan tidak tersambung dengan baik. Dalam lingkungan yang secara osmotik tidak seimbang (seperti di dalam tubuh manusia), air akan masuk ke dalam sel bakteri dengan tekanan tinggi. Dinding sel yang cacat tidak mampu menahan tekanan ini, sehingga sel membengkak dan akhirnya pecah, mengakhiri infeksi.
Perbandingan dengan Antibiotik Spektrum Luas, Antibiotik Spesifik untuk Typhus: Inhibisi Enzim Peptidoglycan
Pendekatan spesifik ini berbeda nyata dengan kerja antibiotik spektrum luas seperti tetrasiklin atau kloramfenikol generasi awal. Antibiotik spektrum luas sering kali bekerja dengan target yang lebih umum, misalnya menghambat sintesis protein pada ribosom 70S, yang dimiliki oleh banyak jenis bakteri, baik patogen maupun komensal yang menguntungkan. Akibatnya, terapi spektrum luas cenderung menyebabkan gangguan mikrobioma usus yang lebih signifikan, meningkatkan risiko diare terkait antibiotik atau infeksi sekunder seperti C. difficile.
Pengembangan antibiotik spesifik untuk typhus yang bekerja dengan menghambat enzim peptidoglycan merupakan terobosan krusial dalam dunia medis. Inovasi ini tidak hanya menyelamatkan nyawa, tetapi juga mendukung produktivitas generasi muda, yang menjadi tulang punggung saat Indonesia Raih Bonus Demografi 2030, Kesejahteraan Tetap Terjaga. Dengan populasi yang sehat dan terlindungi dari ancaman penyakit seperti typhus, bonus demografi dapat benar-benar dimanfaatkan untuk membangun bangsa yang lebih maju dan sejahtera, sekaligus menekan laju resistensi antimikroba.
Sebaliknya, inhibitor enzim peptidoglycan yang dirancang sangat spesifik untuk enzim milik S. typhi memiliki “jangkauan tembak” yang lebih sempit. Ini meminimalkan kerusakan pada flora normal usus, yang merupakan keuntungan besar mengingat typhus adalah infeksi sistemik yang bermula dari saluran cerna. Efek samping sistemik juga berpotensi lebih rendah karena intervensi dilakukan tepat pada mesin pertumbuhan bakteri, bukan pada proses seluler yang mungkin memiliki kemiripan dengan sel inang.
Golongan Antibiotik dan Cara Kerjanya yang Spesifik
Meskipun banyak antibiotik yang memengaruhi sintesis dinding sel, tidak semuanya bersifat spesifik untuk enzim Salmonella typhi. Golongan beta-laktam (seperti penisilin dan sefalosporin) adalah penghambat enzim transpeptidase yang klasik, namun spektrumnya luas. Untuk typhus, penelitian kini berfokus pada pengembangan senyawa yang memiliki afinitas tinggi dan selektivitas terhadap enzim peptidoglycan milik S. typhi, termasuk varian beta-laktam generasi baru dan senyawa non-beta-laktam yang menargetkan langkah-langkah unik dalam biosintesis peptidoglycan bakteri ini.
Pengembangan ini bertujuan untuk mengatasi resistensi yang sudah muncul terhadap terapi lini pertama seperti kloramfenikol, ampisilin, dan kotrimoksazol. Dengan memahami cetak biru molekuler enzim target, para ilmuwan dapat merancang senyawa “kunci pas” yang lebih presisi.
Golongan Penghambat Enzim Peptidoglycan untuk Typhus
Beberapa golongan antibiotik yang telah diteliti atau berpotensi sebagai inhibitor spesifik enzim peptidoglycan pada typhus meliputi sefalosporin generasi ketiga (seperti seftriakson) yang masih luas namun sangat efektif, karbapenem (seperti meropenem) sebagai senjata cadangan, dan senyawa eksperimental yang menargetkan enzim seperti MurA atau MraY yang terlibat dalam tahap awal sintesis. Tabel berikut membandingkan beberapa contoh berdasarkan target dan tahap penghambatannya.
| Nama Antibiotik (Golongan) | Target Enzim Spesifik | Tahap Sintesis Dihambat | Contoh Nama Generik |
|---|---|---|---|
| Sefalosporin Generasi 3 | Penicillin-Binding Protein (PBP, transpeptidase) | Cross-linking (penyilangan) rantai peptida | Seftriakson, Sefotaksim |
| Karbapenem | Multiple Penicillin-Binding Proteins (PBP) | Cross-linking dan mungkin transglycosylasi | Meropenem, Ertapenem |
| Fosfomisin (analog) | Enzim MurA | Tahap sangat awal, pembentukan prekursor NAM | Fosfomisin |
| Muraymycin (senyawa riset) | Enzim MraY (translocase I) | Transfer prekursor peptidoglycan ke lipid carrier | Masih dalam tahap uji praklinis |
Mekanisme Rinci Kerja Seftriakson
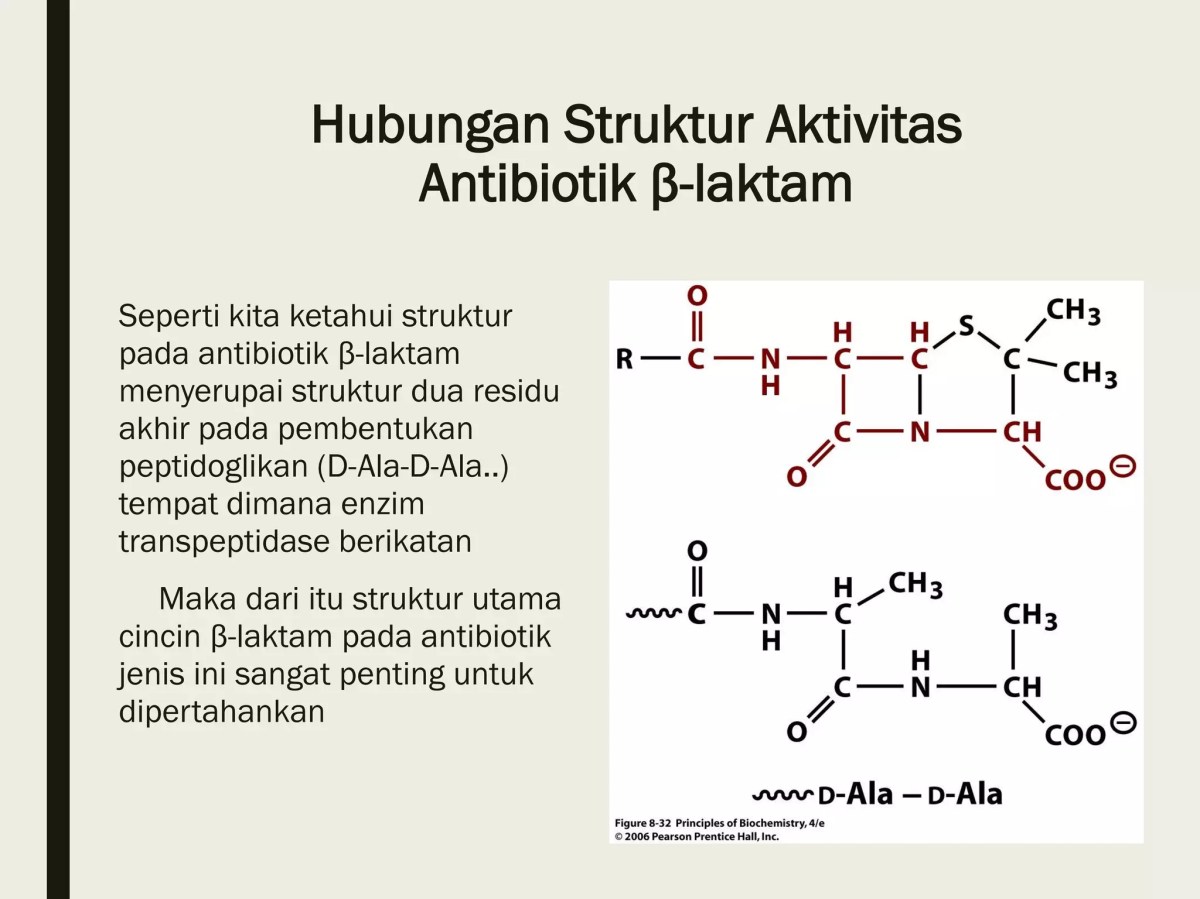
Seftriakson, sebagai contoh yang telah digunakan secara klinis, menunjukkan bagaimana penghambatan spesifik itu bekerja. Molekul seftriakson, dengan inti beta-laktamnya, secara struktural menyerupai bagian D-Ala-D-Ala dari rantai peptida substrat alami. Saat berada di periplasma bakteri, ia berdifusi dan secara kompetitif berikatan dengan situs aktif enzim transpeptidase (PBP).
Pengobatan tifus dengan antibiotik spesifik, seperti yang menargetkan inhibisi enzim peptidoglycan, merupakan intervensi medis yang presisi. Prinsip spesifisitas ini mengingatkan pada nuansa bahasa, sebagaimana terlihat saat Sunarto Beli Sepeda di Pasar Malang, Diterjemah ke Krama Alus , di mana setiap pilihan kata memiliki konteks dan tujuan yang jelas. Demikian pula, selektivitas antibiotik dalam menghambat sintesis dinding sel bakteri Salmonella typhi menjadi kunci efektivitas terapi dan pencegahan resistensi, sebuah pendekatan yang harus dipahami secara mendalam.
Ikatan ini bersifat kovalen dan ireversibel. Enzim yang telah berikatan dengan seftriakson tidak dapat lagi menjalankan fungsinya menyambungkan rantai peptida tetangga. Proses cross-linking peptidoglycan terhenti. Namun, mesin sintesis lainnya, seperti transglycosylase yang merangkai rantai gula, mungkin masih berjalan untuk sementara waktu. Hasilnya adalah produksi dinding sel yang cacat: rantai peptidoglycan yang panjang tetapi tidak tersambung dengan kuat, seperti batu bata yang tidak direkatkan oleh semen.
Dinding sel ini sangat lemah terhadap tekanan osmotik, yang pada akhirnya menyebabkan kematian bakteri.
Keunggulan dan Tantangan dalam Terapi yang Ditargetkan
Beralih ke antibiotik dengan target spesifik enzim peptidoglycan menawarkan janji presisi medis. Keuntungan utamanya terletak pada potensi peningkatan keamanan pasien dan efektivitas terapi. Karena hanya menyerang mekanisme yang sangat vital dan unik bagi bakteri, dampak pada sel manusia dapat diminimalkan, mengurangi kejadian efek samping toksik yang sering dikaitkan dengan obat-obatan lama. Selain itu, dengan dosis yang tepat pada target yang tepat, eliminasi bakteri bisa lebih cepat dan tuntas, berpotensi mempersingkat masa rawat dan menekan angka kekambuhan.
Pengobatan tifus yang efektif kerap melibatkan antibiotik spesifik yang bekerja dengan cara menghambat enzim peptidoglycan transpeptidase, sehingga merusak dinding sel bakteri Salmonella typhi. Prinsip ketepatan target ini, ironisnya, serupa dengan pentingnya ketepatan respons dalam menghadapi konflik sosial, sebagaimana dibahas dalam panduan Cara Menjawab Tuduhan Kasar pada Anak Pesantren. Sama halnya, terapi antibiotik yang tepat sasaran akan memutus siklus infeksi tanpa merusak sel sehat, menekankan bahwa presisi—baik dalam medis maupun pendidikan—adalah kunci resolusi yang otoritatif.
Namun, presisi ini ibarat pedang bermata dua. Spesifisitas tinggi juga berarti bahwa jika targetnya berubah atau bermutasi, senjata yang dirancang sangat spesifik itu bisa menjadi tidak berguna. Inilah tantangan terbesar dari pendekatan ini: resistensi. Bakteri, dengan kemampuan beradaptasinya yang luar biasa, dapat mengembangkan mekanisme untuk mengelak, baik dengan memodifikasi enzim target, memproduksi enzim alternatif, atau meningkatkan efisiensi pompa efflux untuk mengeluarkan obat.
Potensi Perkembangan Resistensi Bakteri
Resistensi terhadap penghambat enzim peptidoglycan dapat muncul melalui beberapa jalan. Mutasi pada gen yang mengkode enzim target (seperti pbp genes) dapat mengubah struktur situs aktif, mengurangi afinitas pengikatan antibiotik tanpa mengganggu fungsi katalitiknya terhadap substrat asli. Bakteri juga dapat memperoleh gen yang memproduksi enzim beta-laktamase, yang secara spesifik memotong cincin beta-laktam sebelum antibiotik sempat berikatan dengan targetnya. Tantangan lainnya adalah perubahan permeabilitas membran luar atau aktivasi sistem pompa yang mengusir obat keluar sel.
Contoh nyata dapat dilihat pada mutasi di gen pbp1A pada beberapa strain Salmonella typhi yang resisten. Mutasi titik (point mutation) yang mengganti asam amino serine dengan arginin pada posisi 83 di situs aktif enzim transpeptidase menyebabkan perubahan konformasi lokal. Perubahan ini mengurangi kemampuan seftriakson untuk berikatan secara erat, sementara substrat alami D-Ala-D-Ala masih dapat diakomodasi. Akibatnya, Minimum Inhibitory Concentration (MIC) obat meningkat signifikan, menandakan penurunan kemanjuran yang drastis.
Prosedur Pengembangan dan Strategi Formulasi: Antibiotik Spesifik Untuk Typhus: Inhibisi Enzim Peptidoglycan
Mengubah sebuah ide tentang inhibitor spesifik menjadi obat yang siap digunakan adalah perjalanan panjang yang membutuhkan metodologi ketat. Prosedur penelitian dimulai dari skrining in vitro untuk mengidentifikasi kandidat senyawa, dilanjutkan dengan optimasi dan validasi sebelum akhirnya diuji pada model hewan dan manusia. Setiap tahap dirancang untuk menjawab pertanyaan spesifik tentang keamanan, efektivitas, dan farmakokinetik senyawa tersebut.
Strategi formulasi menjadi krusial karena antibiotik harus dapat bertahan dari lingkungan asam lambung, diserap dengan baik, didistribusikan ke jaringan yang terinfeksi (termasuk sistem retikuloendotelial tempat S. typhi bersembunyi), dan akhirnya mencapai targetnya di periplasma bakteri dalam konsentrasi yang memadai. Ini memerlukan rekayasa pada tingkat molekuler, seperti memodifikasi gugus kimia untuk meningkatkan stabilitas atau kelarutan.
Prosedur Penelitian In Vitro Awal
Sebelum diuji pada sel atau hewan, potensi senyawa penghambat diukur melalui serangkaian eksperimen biokimia dan mikrobiologi. Garis besar prosedurnya meliputi: pertama, produksi dan pemurnian enzim target rekombinan (misalnya transpeptidase dari S. typhi) dalam sistem ekspresi seperti E. coli. Kedua, pengujian aktivitas enzim dengan substrat sintetis yang memberikan sinyal (misalnya perubahan warna atau fluoresensi) saat diolah. Ketiga, penambahan kandidat senyawa penghambat ke dalam reaksi enzimatik untuk mengukur penurunan aktivitas enzim (IC50).
Keempat, uji mikrodilusi untuk menentukan MIC senyawa terhadap kultur S. typhi hidup, mengkonfirmasi bahwa penghambatan enzim in vitro berhubungan dengan kematian bakteri.
Strategi Formulasi untuk Mencapai Target
Agar antibiotik spesifik dapat menjalankan tugasnya, formulasi harus mengatasi beberapa rintangan biologis. Pertama, obat harus dirancang untuk stabil dalam lingkungan gastrointestinal jika diberikan secara oral, atau kompatibel dengan cairan infus jika parenteral. Kedua, struktur molekul perlu dimodifikasi untuk memastikan distribusi yang memadai ke dalam sel-sel sistem imun seperti makrofag, di mana S. typhi dapat hidup secara intraseluler. Ketiga, senyawa harus memiliki kemampuan menembus membran luar bakteri Gram-negatif, yang sering kali dilengkapi dengan porin yang selektif.
Keempat, formulasi harus mempertimbangkan profil farmakokinetik untuk mempertahankan konsentrasi di atas MIC pada tempat infeksi selama interval dosis.
Tahap Validasi Target Enzim
Sebelum sumber daya besar diinvestasikan untuk pengembangan obat, validasi bahwa suatu enzim memang merupakan target yang layak dan “dapat diobati” (druggable) adalah langkah kritis. Validasi ini dilakukan melalui pendekatan genetik dan kimia.
- Validasi Genetik: Menggunakan teknik seperti knock-out gen atau RNA interference (jika memungkinkan) untuk menonaktifkan gen enzim target pada bakteri. Jika penghambatan genetik ini menyebabkan kematian bakteri atau menghambat pertumbuhan yang parah, itu menunjukkan bahwa enzim tersebut esensial untuk kelangsungan hidup bakteri, menjadikannya target yang menarik.
- Validasi Kimia: Menunjukkan bahwa senyawa kimia kecil yang diketahui berikatan dengan enzim tersebut dapat meniru efek penghambatan genetik, yaitu membunuh atau menghambat pertumbuhan bakteri. Ini membuktikan bahwa target dapat diakses dan dimodulasi oleh molekul obat.
- Validasi Mekanistik: Membuktikan bahwa efek bakterisidal dari senyawa kimia tersebut memang secara langsung disebabkan oleh penghambatan enzim target, dan bukan melalui target lain (off-target effects). Ini dapat dilakukan dengan menunjukkan bahwa mutasi pada enzim target menyebabkan resistensi terhadap senyawa tersebut.
Bukti Empiris dari Studi Klinis dan Pra-Klinis
Dukungan untuk pendekatan spesifik ini tidak hanya datang dari teori, tetapi juga dari data eksperimental dan klinis yang mulai bermunculan. Studi pra-klinis pada model hewan yang diinfeksi strain S. typhi multi-drug resistant (MDR) atau extensively drug-resistant (XDR) menunjukkan bahwa senyawa penghambat enzim peptidoglycan yang baru, seperti beberapa derivat beta-laktam atau senyawa yang menargetkan MraY, mampu membersihkan infeksi dengan efisiensi yang mengesankan.
Studi klinis, meski masih terbatas, sering kali membandingkan obat-obatan seperti seftriakson (yang relatif lebih spesifik untuk PBP) dengan antibiotik spektrum luas yang lebih tua.
Data dari studi-studi ini memberikan gambaran tentang parameter keberhasilan terapi, seperti waktu yang dibutuhkan untuk menurunkan demam (defervescence), angka kesembuhan mikrobiologis, dan kemungkinan kambuh. Parameter-parameter ini menjadi tolok ukur objektif untuk menilai apakah terapi yang lebih ditargetkan memberikan manfaat klinis yang nyata.
Temuan Data Perbandingan Terapi
Source: slidesharecdn.com
Sebagai ilustrasi, data komparatif dari beberapa studi observasional dan uji klinis fase III dapat diringkas untuk memberikan gambaran. Perlu dicatat bahwa angka-angka berikut adalah ilustrasi berdasarkan tren yang dilaporkan dalam literatur, dan dapat bervariasi tergantung strain dan populasi pasien.
| Parameter Terapi | Terapi Konvensional (misal, Kloramfenikol) | Terapi Spesifik (misal, Seftriakson) | Keterangan |
|---|---|---|---|
| Angka Kesembuhan Mikrobiologis (Hari 7) | ~70-80% | ~90-95% | Kesembuhan didefinisikan sebagai kultur darah negatif. |
| Waktu Rata-rata Defervescence (Hari) | 5 – 7 hari | 3.5 – 5 hari | Waktu hingga suhu tubuh normal stabil. |
| Relapse Rate (Kekambuhan) | ~5-10% | ~1-3% | Infeksi muncul kembali setelah pengobatan dihentikan. |
| Kejadian Efek Samping Hepatotoksik | Lebih tinggi | Lebih rendah | Terutama relevan untuk kloramfenikol. |
Visualisasi Interaksi Antibiotik-Enzim
Pemahaman mendalam tentang bagaimana antibiotik berikatan dengan enzim targetnya sering kali diperoleh dari visualisasi struktur 3D menggunakan teknik seperti kristalografi sinar-X. Bayangkan sebuah model komputer yang menunjukkan struktur enzim transpeptidase dari S. typhi. Enzim ini digambarkan sebagai pita berwarna-warni yang melipat dan berbelit, membentuk sebuah ceruk atau lekukan yang merupakan situs aktifnya. Di dalam ceruk ini, molekul seftriakson terlihat terikat dengan erat, seperti kunci yang masuk ke dalam gembok.
Bagian inti beta-laktam dari seftriakson terletak persis di posisi di mana substrat alami (D-Ala-D-Ala) akan dipotong. Atom-atom oksigen dan nitrogen pada cincin beta-laktam membentuk jaringan ikatan hidrogen dan interaksi elektrostatik dengan residu asam amino spesifik (seperti serine dan lisin) di dinding situs aktif. Ekor molekul seftriakson yang lebih panjang memanjang keluar dari ceruk, berinteraksi dengan area lain pada permukaan enzim, yang meningkatkan kekuatan dan spesifisitas pengikatan.
Visualisasi ini bukan hanya gambar statis; ia menjelaskan secara atom-by-atom mengapa obat ini efektif dan bagaimana mutasi dapat menggeser posisi atom-atom kunci tersebut, sehingga merusak interaksi dan menyebabkan resistensi.
Implikasi pada Penanganan Klinis dan Panduan ke Depan
Adanya antibiotik dengan target spesifik yang efektif terhadap strain resisten akan mengubah peta penanganan typhus, terutama di daerah endemik. Protokol yang selama ini mengandalkan obat lini pertama yang sudah mulai tumpul daya tahannya dapat diperbarui. Prioritasnya adalah menyelamatkan nyawa dengan terapi yang lebih dapat diandalkan, sekaligus mengurangi durasi penularan dengan mempercepat penyembuhan. Implikasinya juga administratif: kebutuhan akan tes diagnostik cepat yang dapat mendeteksi pola resistensi mungkin akan meningkat untuk memandu pemilihan terapi yang tepat sejak awal.
Di tingkat pelayanan kesehatan dasar, keberadaan obat yang lebih aman dan dengan regimen dosis yang mungkin lebih sederhana (misalnya sekali sehari) dapat meningkatkan kepatuhan pasien dan mempermudah logistik pengobatan. Namun, ini harus diimbangi dengan sistem pemantauan yang baik untuk mendeteksi secara dini jika resistensi terhadap senjata baru ini mulai muncul.
Panduan Pemantauan Pasien
Penerapan terapi berbasis inhibisi spesifik memerlukan panduan klinis yang jelas untuk memastikan keselamatan dan efektivitas maksimal. Draft poin-poin panduan pemantauan dapat mencakup: pertama, pemantauan klinis ketat terhadap suhu dan gejala sistemik selama 3-5 hari pertama untuk menilai respons. Kedua, pemeriksaan kultur darah ulang pada titik waktu tertentu (misalnya hari ke-3 dan 7) untuk memastikan sterilisasi, terutama pada kasus berat atau immunocompromised.
Ketiga, pemantauan fungsi hati dan ginjal secara berkala, meski efek samping hepatotoksik lebih rendah, sebagai tindakan kehati-hatian standar. Keempat, edukasi kepada pasien tentang pentingnya menyelesaikan seluruh regimen pengobatan meskipun sudah merasa sehat, untuk mencegah kekambuhan dan seleksi bakteri resisten. Kelima, pelaporan yang sistematis terhadap setiap kasus kegagalan terapi atau kekambuhan dini ke otoritas kesehatan, sebagai sistem peringatan dini untuk resistensi.
Masa Depan Terapi Kombinasi
Untuk memperpanjang masa manfaat antibiotik spesifik dan mengatasi kompleksitas infeksi intraseluler S. typhi, terapi kombinasi menjadi proyeksi yang logis. Masa depan mungkin melihat kombinasi inhibitor enzim peptidoglycan dengan agen antimikroba lain yang memiliki mekanisme berbeda. Contohnya, menggabungkan seftriakson (penghambat sintesis dinding sel) dengan azitromisin (penghambat sintesis protein pada ribosom 50S) dapat menghasilkan efek sinergis atau setidaknya aditif, membunuh bakteri melalui dua front sekaligus dan menyulitkan perkembangan resistensi.
Kombinasi lain yang sedang diteliti adalah dengan senyawa yang menargetkan metabolisme folat atau dengan bakteriofag terapeutik. Strategi “menyerang dari banyak sisi” ini diharapkan dapat meningkatkan kecepatan penyembuhan, mengurangi dosis masing-masing obat, dan yang terpenting, menjadi batu sandungan yang lebih besar bagi bakteri untuk mengembangkan resistensi.
Simpulan Akhir
Dari paparan di atas, terlihat jelas bahwa pendekatan inhibisi enzim peptidoglycan menawarkan presisi yang belum pernah ada sebelumnya dalam memerangi typhus. Meski tantangan seperti resistensi tetap harus diwaspadai, fondasi ilmiah yang kuat dan data pendukung yang menjanjikan membuka jalan bagi terapi yang lebih rasional. Ke depan, kombinasi antibiotik spesifik ini dengan agen lain berpotensi menciptakan rejimen pengobatan yang lebih tangguh, mengurangi beban penyakit di daerah endemik, dan pada akhirnya menyelamatkan lebih banyak nyawa dengan cara yang lebih cerdas dan efisien.
Pertanyaan yang Kerap Ditanyakan
Apakah antibiotik spesifik ini sudah tersedia dan bisa diresepkan dokter?
Belum. Sebagian besar masih dalam tahap penelitian dan pengembangan klinis. Antibiotik yang saat ini umum diresepkan untuk typhus, seperti kloramfenikol atau seftriakson, masih merupakan pilihan utama.
Bagaimana cara mengetahui bakteri typhus pada pasien sensitif terhadap antibiotik jenis ini?
Diperlukan tes sensitivitas atau uji genetik khusus di laboratorium mikrobiologi yang canggih untuk mendeteksi keberadaan enzim target yang masih rentan, sebelum memutuskan penggunaan terapi spesifik.
Apakah terapi ini akan membuat harga pengobatan typhus menjadi lebih mahal?
Sangat mungkin pada awal peluncurannya, karena melibatkan teknologi pengembangan obat yang kompleks. Namun, dalam jangka panjang, efektivitasnya yang tinggi dapat mengurangi durasi rawat inap dan risiko komplikasi, yang berpotensi menurunkan biaya perawatan secara keseluruhan.
Bisakah anak-anak atau ibu hamil menggunakan antibiotik dengan mekanisme kerja seperti ini?
Keamanan pada kelompok populasi khusus akan menjadi bagian penting dari uji klinis fase lanjutan. Prinsipnya, karena targetnya spesifik bakteri, secara teori lebih aman, namun keputusan penggunaannya tetap harus menunggu hasil evaluasi keamanan yang komprehensif.