Perbaikan Mutan akibat UV dan Mekanismenya adalah cerita detektif molekuler yang terjadi setiap hari di dalam tubuh kita, sebuah pertarungan tak kasat mata untuk menjaga keutuhan cetak biru kehidupan. Setiap kali kulit terpapar sinar matahari, radiasi ultraviolet membombardir DNA sel, menciptakan kerusakan yang berpotensi memicu mutasi. Namun, alam telah melengkapi sel dengan mekanisme perbaikan yang canggih dan teliti, bagaikan tim teknisi ahli yang selalu siaga memperbaiki kesalahan dalam kode genetik sebelum berubah menjadi masalah serius.
Dari enzim fotolase yang menggunakan energi cahaya untuk memperbaiki kerusakan secara langsung, hingga sistem kompleks seperti Nucleotide Excision Repair yang memotong dan mengganti segmen DNA yang rusak, sel memiliki arsenal pertahanan yang berlapis. Memahami mekanisme ini bukan hanya tentang mengungkap keajaiban biologi seluler, tetapi juga membuka kunci untuk memahami penyakit seperti kanker kulit hingga mengembangkan strategi bioteknologi yang inovatif.
Dasar-Dasar Mutasi dan Radiasi UV
Setiap hari, DNA di dalam sel-sel kita menghadapi serangan dari berbagai agen perusak, baik dari dalam tubuh maupun lingkungan luar. Salah satu ancaman paling konstan dan universal adalah radiasi ultraviolet (UV) dari matahari. Mutasi genetik, yang merupakan perubahan pada urutan basa nitrogen DNA, dapat terjadi ketika kerusakan akibat UV ini tidak diperbaiki dengan baik. Radiasi UV berperan sebagai mutagen fisik yang energinya cukup tinggi untuk menginduksi perubahan kimiawi langsung pada molekul DNA, berbeda dengan mutagen kimia yang bereaksi secara spesifik.
Spektrum radiasi UV dibagi berdasarkan panjang gelombang dan energi yang dibawanya. UVA (320-400 nm) memiliki energi terendah dan sebagian besar diserap oleh komponen sel selain DNA, namun dapat menyebabkan kerusakan tidak langsung melalui pembentukan radikal bebas. UVB (280-320 nm) adalah pemicu utama kerusakan DNA secara langsung dan paling bertanggung jawab atas efek karsinogenik sinar matahari. Sementara UVC (100-280 nm) memiliki energi tertinggi dan paling merusak, namun secara alami disaring oleh lapisan ozon atmosfer bumi sehingga tidak mencapai permukaan.
Struktur DNA Rentan dan Jenis Kerusakan UV
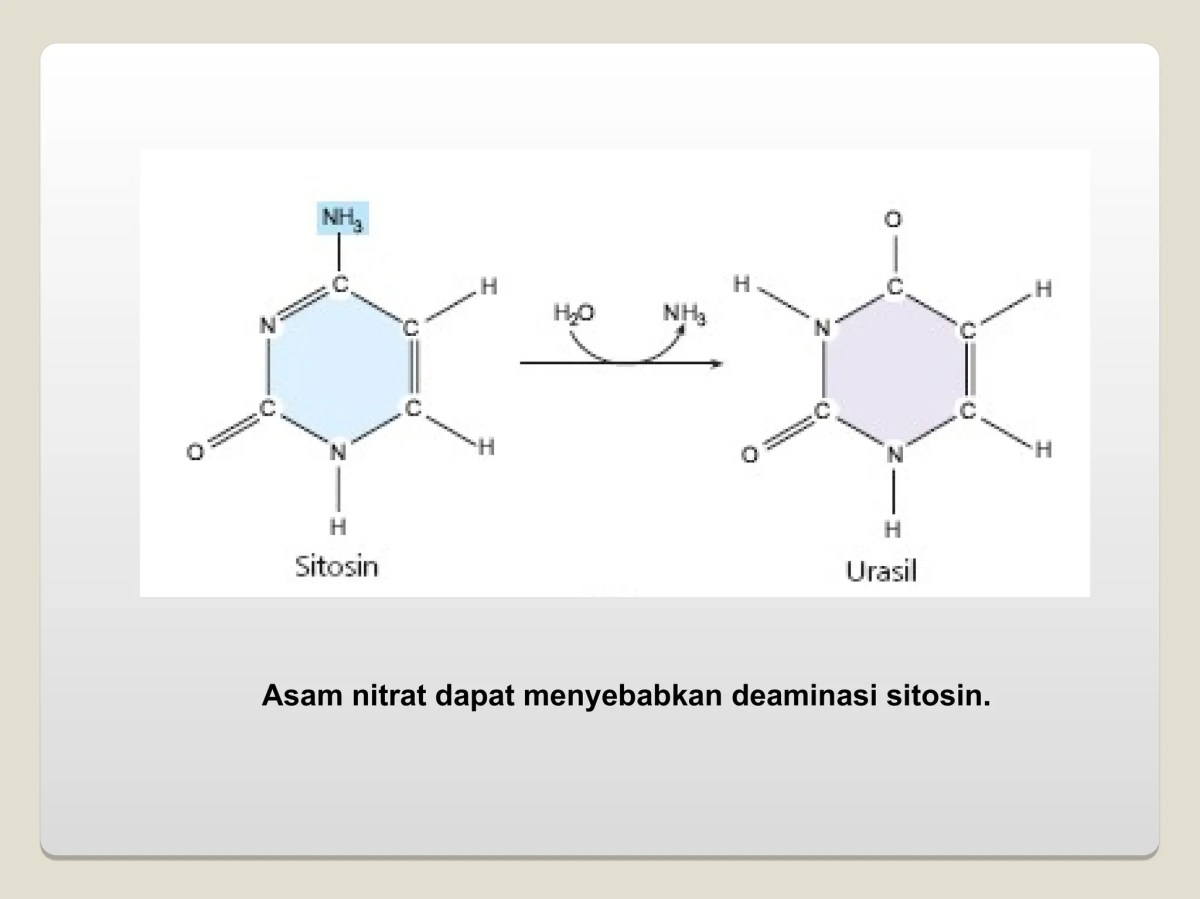
Molekul DNA memiliki titik lemah tertentu terhadap serangan UV. Basa nitrogen, khususnya pirimidin (sitosin dan timin), sangat rentan karena struktur cincinnya yang dapat menyerap energi radiasi UV. Ketika dua pirimidin yang berdekatan dalam untai DNA yang sama terpapar UV, mereka dapat membentuk ikatan kovalen yang tidak normal. Struktur paling rentan adalah sekuens DNA yang kaya akan pasangan basa timin-adenin (T-A) atau sitosin-guanin (C-G) yang berurutan.
Berikut adalah tabel yang merangkum jenis kerusakan DNA utama akibat radiasi UV, beserta contoh dan konsekuensinya.
| Jenis Kerusakan | Contoh Spesifik | Mekanisme Terbentuk | Konsekuensi Potensial |
|---|---|---|---|
| Dimer Pirimidin | Dimer Siklobutana (CPD), Dimer Pirimidin (6-4) | Ikatan kovalen antar dua basa pirimidin berdekatan (TT, TC, CT, CC) pada untai yang sama. | Distorsi heliks ganda, menghalangi replikasi & transkripsi, titik mutasi tetap jika tidak diperbaiki. |
| Produk Fotooksidasi | 8-oxoguanine (8-oxoG) | Oksidasi basa guanin oleh radikal bebas yang diinduksi UVA. | Mismatch dengan adenin selama replikasi, menyebabkan transisi mutasi G:C ke T:A. |
| Pemutusan Untai DNA | Pemutusan Untai Tunggal (SSB) | Kerusakan basa yang labil atau aktivitas enzim perbaikan yang tidak sempurna. | Dapat berkembang menjadi pemutusan untai ganda (DSB) selama replikasi, sangat berbahaya bagi stabilitas genom. |
| Crosslink DNA-Protein | Ikatan antara DNA dan protein histon atau enzim | Pembentukan ikatan kovalen antara DNA dan protein terdekat akibat radiasi UV. | Menghalangi proses seluler vital yang membutuhkan akses ke DNA, seperti replikasi dan transkripsi. |
Mekanisme Perbaikan DNA Pencahayaan (Photoreactivation)
Source: slidesharecdn.com
Di antara berbagai sistem perbaikan DNA, terdapat satu mekanisme yang benar-benar elegan dan langsung: perbaikan pencahayaan atau photoreactivation. Mekanisme ini unik karena bergantung pada cahaya tampak (biru hingga UV-A) sebagai sumber energi untuk membalikkan kerusakan secara langsung, tanpa perlu memotong atau mensintesis ulang bagian DNA yang rusak. Ini adalah contoh langka perbaikan enzimatik yang bersifat “fotoreseptif”.
Peran Enzim Fotolase
Enzim kunci dalam proses ini adalah fotolase, sebuah flavoprotein yang mengandung kofaktor penangkap cahaya. Fotolase bekerja dengan sangat spesifik menargetkan dimer pirimidin, terutama dimer siklobutana. Cara kerjanya dapat dideskripsikan dalam tiga tahap berurutan. Pertama, enzim fotolase secara difusif mengikat ke lokasi DNA yang mengandung dimer pirimidin, mengenali distorsi pada struktur heliks. Kedua, setelah terikat, kofaktor dalam enzim (biasanya metilen tetrahidrofolat dan FADH-) menyerap foton cahaya tampak (panjang gelombang 300-500 nm).
Energi cahaya ini kemudian ditransfer ke dimer pirimidin. Tahap ketiga, energi yang diserap digunakan untuk memutuskan ikatan kovalen siklik yang salah antara dua basa pirimidin, sehingga mengembalikannya ke bentuk monomerik normal secara kimiawi dan reversibel.
Distribusi dan Keterbatasan Fotoreaktivasi
Meski efisien dan tanpa kesalahan, mekanisme ini tidak universal. Fotoreaktivasi ditemukan pada banyak bakteri, archaea, protista, fungi, tumbuhan, dan sebagian besar hewan non-mamalia. Namun, mekanisme ini secara mencolok tidak ditemukan pada mamalia plasenta, termasuk manusia. Hilangnya jalur ini selama evolusi mamalia masih menjadi bahan studi, namun diduga terkait dengan adaptasi kehidupan nokturnal leluhur atau redundansi dengan sistem perbaikan eksisi yang lebih kompleks.
Fotoreaktivasi adalah satu-satunya sistem perbaikan DNA yang sepenuhnya bergantung pada cahaya sebagai kofaktor. Kehilangan mekanisme langsung dan tanpa kesalahan ini pada mamalia menjadikan kita lebih bergantung pada sistem perbaikan eksisi yang kompleks dan berisiko menghasilkan kesalahan, yang mungkin berkontribusi pada kerentanan kita terhadap kanker kulit.
Mekanisme Perbaikan Eksisi Nukleotida (Nucleotide Excision Repair/NER): Perbaikan Mutan Akibat UV Dan Mekanismenya
Untuk mengatasi kerusakan berat yang menyebabkan distorsi besar pada heliks DNA, seperti dimer pirimidin, sel mengandalkan mekanisme perbaikan eksisi nukleotida (NER). NER adalah sistem perbaikan serba guna yang sangat penting dan kompleks, sering disebut sebagai “pemotong dan penambal” molekuler. Berbeda dengan photoreactivation yang langsung, NER melibatkan pemotongan segmen oligonucleotida yang mengandung kerusakan dan mensintesis ulang bagian tersebut menggunakan untai komplemen sebagai cetakan.
Alur Mekanisme NER pada Eukariota
Proses NER pada sel eukariota melibatkan koordinasi puluhan protein dalam tahapan yang teratur. Awalnya, kompleks pendeteksi kerusakan, seperti XPC-RAD23B dan DDB1-DDB2 (untuk kerusakan UV), mengenali distorsi heliks dan mengikat lokasi tersebut. Kemudian, kompleks transkripsi faktor TFIIH yang mengandung helikase (XPB dan XPD) direkrut untuk membuka heliks DNA di sekitar kerusakan. Protein XPA dan RPA kemudian menstabilkan gelembung transkripsi ini. Selanjutnya, enzim endonuklease (XPF-ERCC1 dan XPG) memotong untai DNA yang rusak pada posisi sekitar 20-30 nukleotida di hulu dan 5-6 nukleotida di hilir kerusakan.
Mekanisme perbaikan mutan akibat radiasi UV melibatkan kompleksitas sistem seluler yang luar biasa, serupa dengan bagaimana manusia berusaha memahami tanda-tanda spiritual yang agung. Dalam konteks ini, pencarian ciri-ciri khusus, seperti upaya mengenali Ciri Malam Lailatul Qadr Seperti Apa , memerlukan ketelitian dan kepekaan tersendiri. Demikian pula, identifikasi dan koreksi kerusakan DNA membutuhkan presisi enzimatik yang otoritatif untuk memulihkan integritas genetik secara sempurna.
Segmen DNA yang mengandung kerusakan kemudian dilepaskan, meninggalkan celah. Celah ini diisi oleh DNA polimerase (δ/ε) yang disertai faktor prosesivitas PCNA, menggunakan untai komplemen yang sehat sebagai cetakan. Terakhir, enzim ligase (Ligase I atau III) menyambungkan ujung nukleotida baru dengan tulang punggung DNA yang lama.
Jalur Global dan Terikat Transkripsi, Perbaikan Mutan akibat UV dan Mekanismenya
Sistem NER beroperasi melalui dua sub-jalur utama yang memiliki target dan efisiensi berbeda:
- NER Global Genome (GG-NER): Berjalan di seluruh genom, termasuk daerah yang tidak aktif ditranskripsi. Jalur ini bergantung pada kompleks XPC untuk inisiasi deteksi dan relatif lebih lambat. GG-NER adalah pertahanan utama terhadap kerusakan akibat UV pada daerah genomik non-coding.
- NER Terikat Transkripsi (TC-NER): Secara khusus memperbaiki kerusakan pada untai DNA yang sedang aktif ditranskripsi. Inisiasi dipicu oleh terhentinya RNA polimerase II di hadapan kerusakan. Jalur ini lebih cepat dan diprioritaskan untuk memastikan kelangsungan ekspresi gen yang vital.
Meski memiliki prinsip dasar yang sama, implementasi NER pada prokariota (seperti bakteri E. coli) dan eukariota memiliki perbedaan signifikan dalam kompleksitas protein yang terlibat.
| Karakteristik | NER pada Prokariota (E. coli) | NER pada Eukariota (Manusia) |
|---|---|---|
| Kompleks Protein | Relatif sederhana, intinya adalah kompleks UvrA, UvrB, UvrC, UvrD. | Sangat kompleks, melibatkan >30 protein (XPA, XPC, TFIIH, RPA, dll). |
| Pengenalan Kerusakan | Dilakukan oleh dimer UvrA yang berjalan di sepanjang DNA, bersama UvrB. | Multi-step, melibatkan XPC-RAD23B untuk GG-NER dan RNA pol II stall untuk TC-NER. |
| Panjang Eksisi | Segmen pendek, sekitar 12-13 nukleotida. | Segmen lebih panjang, sekitar 24-32 nukleotida. |
| Regulasi dan Keterkaitan | Lebih terisolasi sebagai sistem khusus. | Terkait erat dengan proses transkripsi, replikasi, dan siklus sel. |
Mekanisme Perbaikan Mismatch dan Sistem Pendukung Lainnya
Selain menangani kerusakan langsung dari UV, sel juga harus waspada terhadap kesalahan yang mungkin timbul sebagai konsekuensi tidak langsung selama proses perbaikan DNA itu sendiri. Mekanisme perbaikan mismatch (MMR) berfungsi sebagai “proofreader” atau korektor akhir yang memastikan integritas urutan basa setelah proses seperti sintesis ulang selama NER atau replikasi DNA normal.
Kontribusi MMR dalam Konteks Perbaikan UV
Sistem MMR terutama dikerahkan untuk memperbaiki kesalahan pasangan basa (mismatch) dan loop penyisipan/deleksi kecil yang lolos dari proofreading DNA polimerase. Dalam konteks perbaikan kerusakan UV, setelah NER melakukan sintesis ulang untuk mengisi celah, ada kemungkinan kecil DNA polimerase memasukkan basa yang salah. Sistem MMR, yang dikenali oleh protein seperti MSH2-MSH6 (MutSα), akan mendeteksi mismatch tersebut, membedakan untai baru (yang mengandung kesalahan) dari untai cetakan lama (yang sudah diperiksa), kemudian mengeskisi segmen dari untai baru dan mensintesis ulang.
Dengan demikian, MMR dan NER bekerja secara sinergis; NER menghilangkan lesi fisik, sementara MMR meminimalkan mutasi titik yang mungkin timbul dari proses perbaikan tersebut.
Perbaikan mutan akibat radiasi UV bergantung pada mekanisme enzimatik yang kompleks, mirip cara kita perlu ketelitian saat Hitung Jumlah Lembar Rp50.000 dari Total Rp13,2 Juta dengan Rasio 4:3:2:1. Proses perhitungan rasio yang presisi itu analog dengan kerja sistem seluler yang memulihkan DNA secara proporsional, di mana setiap komponen memiliki porsi peran yang krusial untuk memastikan integritas genetik tetap terjaga.
Perbandingan efektivitas dan target utama antara NER dan MMR cukup jelas. NER adalah garis depan pertahanan spesifik terhadap distorsi heliks besar akibat kerusakan kimia/fisik seperti dimer UV. Sementara MMR adalah sistem penjamin kualitas yang menjaga ketepatan replikasi dan perbaikan, targetnya adalah kesalahan pasangan basa dalam DNA heliks normal. Kegagalan NER menyebabkan akumulasi lesi yang menghalangi proses sel, sedangkan kegagalan MMR menyebabkan peningkatan laju mutasi spontan di seluruh genom.
Mekanisme Perbaikan Alternatif dan Darurat
Ketika sistem perbaikan utama kewalahan atau tidak tersedia, sel memiliki opsi darurat. Mekanisme ini sering kali toleran terhadap kesalahan (error-prone) tetapi lebih baik daripada membiarkan kerusakan tidak teratasi yang dapat mematikan sel.
- Translasi Sintesis (Translesion Synthesis/TLS): DNA polimerase khusus (seperti Pol η pada manusia) yang dapat melewati lesi seperti dimer timin tanpa berhenti, meski dengan risiko memasukkan basa yang salah. Pol η justru sering memasukkan dua adenin di seberang dimer timin dengan akurasi cukup baik, menjadikannya penting untuk mencegah mutasi akibat UV.
- Rekombinasi Homolog (HR) dan End Joining: Untuk kerusakan yang parah seperti pemutusan untai ganda (DSB) yang mungkin timbul dari upaya perbaikan yang gagal atau replikasi di atas lesi yang belum diperbaiki. HR menggunakan kromatid saudara sebagai cetakan untuk perbaikan yang akurat, sementara Non-Homologous End Joining (NHEJ) langsung menyambungkan ujung DNA yang patah namun berisiko menyebabkan delesi atau insersi.
Implikasi Biologis dan Studi Kasus
Pentingnya sistem perbaikan DNA ini menjadi sangat nyata ketika kita melihat konsekuensi ketika sistem tersebut gagal berfungsi. Studi tentang ketidakmampuan perbaikan DNA tidak hanya menjelaskan patologi penyakit langka, tetapi juga memberikan wawasan mendasar tentang mekanisme karsinogenesis pada populasi umum.
Xeroderma Pigmentosum: Contoh Konsekuensi Kegagalan NER
Xeroderma Pigmentosum (XP) adalah penyakit genetik autosomal resesif yang menjadi bukti nyata betapa krusialnya sistem NER bagi kelangsungan hidup. Penderita XP memiliki mutasi pada salah satu dari gen-gen yang mengkode protein inti NER (XPA hingga XPG, atau gen Pol η/TLS). Akibatnya, sel-sel mereka tidak mampu memperbaiki kerusakan DNA akibat UV dengan efektif. Individu dengan XP mengalami fotosensitivitas ekstrem, menunjukkan luka bakar parah akibat paparan sinar matahari minimal, dan memiliki risiko berkembangnya kanker kulit (seperti melanoma dan karsinoma sel basal) yang meningkat hingga 10.000 kali lipat, seringkali muncul sebelum usia 10 tahun.
Kondisi ini dengan jelas mendemonstrasikan hubungan sebab-akibat langsung antara akumulasi kerusakan DNA UV, kegagalan perbaikan, dan inisiasi kanker.
Ekstremofil dan Aplikasi Bioteknologi
Di sisi lain alam, organisme ekstremofil yang hidup di lingkungan dengan radiasi UV tinggi, seperti Deinococcus radiodurans (bakteri yang terkenal tahan radiasi) dan cyanobacteria di dataran tinggi Andes, telah mengembangkan sistem perbaikan DNA yang sangat efisien. D. radiodurans, misalnya, tidak hanya memiliki NER yang sangat aktif, tetapi juga kemampuan rekombinasi homolog yang luar biasa cepat dan akurat untuk menyatukan kembali genomnya yang terfragmentasi.
Memahami mekanisme ini menginspirasi bidang bioteknologi, seperti pengembangan enzim perbaikan yang lebih stabil untuk digunakan dalam diagnostik molekuler, atau rekayasa tanaman dengan ketahanan UV lebih tinggi.
Penelitian tentang perbaikan DNA akibat UV juga merupakan inti dari onkologi modern. Banyak kemoterapi dan terapi radiasi bekerja dengan sengaja menyebabkan kerusakan DNA pada sel kanker yang cepat membelah. Memahami bagaimana sel normal memperbaiki kerusakan tersebut membantu merancang strategi untuk melindungi jaringan sehat. Selain itu, inhibitor terhadap protein perbaikan DNA tertentu (seperti PARP inhibitor) kini digunakan sebagai terapi presisi untuk kanker dengan latar belakang defek pada jalur perbaikan lain (seperti mutasi BRCA pada kanker payudara dan ovarium), sebuah konsep yang dikenal sebagai “sintetik letal”.
Studi pada tahun 2020 yang diterbitkan dalam Nature Communications menunjukkan bahwa enzim fotolase dari mikroorganisme tertentu dapat diintroduksi ke dalam sel kulit manusia di laboratorium dan, ketika diaktifkan dengan cahaya biru, secara signifikan meningkatkan perbaikan dimer pirimidin. Temuan ini membuka pintu untuk pendekatan terapi gen atau enzim topikal potensial dalam pencegahan kanker kulit, meski masih dalam tahap penelitian awal.
Akhir Kata
Dengan demikian, narasi tentang Perbaikan Mutan akibat UV dan Mekanismenya menegaskan bahwa kehidupan pada intinya adalah tentang ketahanan dan presisi. Sistem perbaikan DNA bukan sekadar fitur tambahan, melainkan fondasi esensial yang memungkinkan organisme bertahan di bawah teriknya matahari. Ketika sistem ini gagal, seperti pada penderita Xeroderma Pigmentosum, konsekuensinya sangat nyata. Namun, kisah sukses dari organisme ekstremofil yang tangguh memberikan harapan dan inspirasi.
Pada akhirnya, mempelajari mekanisme perbaikan ini adalah mempelajari seni bertahan hidup pada tingkat molekuler, sebuah pengetahuan yang terus membuka jalan bagi terapi medis dan inovasi sains masa depan.
Mekanisme perbaikan mutan akibat radiasi UV, seperti fotoreaktivasi dan eksisi nukleotida, menunjukkan ketangguhan biologis dalam mengatasi kerusakan. Ketangguhan adaptif ini mengingatkan pada kompleksitas tantangan kolektif di tingkat regional, sebagaimana dijelaskan dalam analisis mendalam mengenai Faktor Penghambat Kerja Sama ASEAN: Kebijakan Protektif, Ideologi, Geografi, Iklim, Sumber Daya. Persoalan geopolitik tersebut, meski skalanya berbeda, sama-sama memerlukan mekanisme koordinasi yang presisi untuk mencapai stabilitas, sebuah prinsip yang juga tercermin dalam efisiensi sistem perbaikan DNA seluler menghadapi tekanan lingkungan.
Panduan Tanya Jawab
Apakah semua kerusakan DNA akibat UV bisa diperbaiki?
Tidak selalu 100%. Meskipun sel memiliki beberapa sistem perbaikan yang tumpang tindih, kerusakan yang sangat masif atau letaknya spesifik dapat terlewat. Akumulasi kerusakan yang tidak terperbaiki inilah yang menjadi pemicu utama mutasi permanen dan penuaan sel.
Mengapa manusia tidak memiliki mekanisme fotoreaktivasi (fotolase)?
Alasan pastinya masih diteliti, tetapi diduga karena mamalia mengandalkan sistem perbaikan yang lebih kompleks seperti NER yang dapat menangani berbagai jenis kerusakan, tidak hanya yang disebabkan oleh UV. Evolusi mungkin menganggap sistem seperti NER lebih menguntungkan untuk organisme dengan genom yang besar dan kompleks.
Bagaimana paparan UV dari gadget atau lampu neon mempengaruhi DNA?
Kebanyakan gadget dan lampu neon modern dirancang untuk memancarkan sangat sedikit atau tidak ada radiasi UV. Risiko kerusakan DNA dari sumber ini secara umum jauh lebih rendah dibandingkan paparan langsung sinar matahari. Namun, paparan intens dan jangka panjang terhadap sumber cahaya tertentu yang memancarkan UVA/UVB tetap berpotensi menimbulkan kerusakan.
Apakah kemampuan perbaikan DNA bisa ditingkatkan?
Secara alami, kemampuan ini ditentukan oleh genetika. Penelitian sedang berfokus pada cara untuk mendukung atau “mengerek” aktivitas enzim perbaikan DNA, misalnya melalui senyawa tertentu atau terapi gen, terutama untuk kondisi seperti Xeroderma Pigmentosum. Gaya hidup sehat seperti diet kaya antioksidan juga diduga membantu mendukung lingkungan seluler yang optimal untuk perbaikan.