Protein bersifat amfoter: bereaksi dengan asam dan basa adalah kunci untuk membuka rahasia bagaimana molekul penting kehidupan ini beroperasi dan berinteraksi dengan lingkungan kimianya. Sifat fundamental ini bukan hanya teori laboratorium, tetapi merupakan prinsip aktif yang mengatur segala sesuatu mulai dari tekstur makanan hingga fungsi enzim dalam tubuh Anda. Memahaminya memberikan wawasan mendalam tentang dunia biokimia yang kompleks dan elegan.
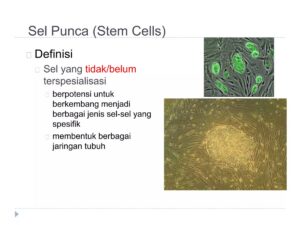
Inti dari sifat amfoter protein terletak pada strukturnya yang unik, yang mengandung kedua gugus asam (karboksil, -COOH) dan basa (amino, -NH₂). Dualitas ini memungkinkan protein bertindak sebagai asam dengan mendonorkan proton dalam lingkungan basa, atau sebagai basa dengan menerima proton dalam lingkungan asam. Kemampuan beradaptasi inilah yang menjadikan protein sangat penting untuk proses biologis, memengaruhi muatan, kelarutan, dan stabilitasnya berdasarkan kondisi pH sekitarnya.
Pengertian dan Konsep Dasar Sifat Amfoter pada Protein
Sifat amfoter merupakan konsep kimia yang menarik, menggambarkan kemampuan suatu zat untuk bertindak sebagai asam atau basa, tergantung pada lingkungannya. Dalam dunia biomolekul, sifat ini sangat penting, terutama untuk protein yang memainkan peran sentral dalam hampir semua proses biologis. Memahami sifat amfoter protein membuka jendela untuk memahami perilakunya dalam tubuh dan berbagai aplikasi industri.
Protein bersifat amfoter artinya molekul protein dapat menerima proton (H⁺) sehingga bersifat sebagai basa, atau melepas proton sehingga bersifat sebagai asam. Kemampuan dualistik ini bersumber langsung dari struktur dasarnya. Protein tersusun dari rantai asam amino, dan setiap asam amino memiliki setidaknya dua gugus fungsional kunci: gugus amina (-NH₂) yang dapat menerima proton menjadi -NH₃⁺, dan gugus karboksilat (-COOH) yang dapat melepas proton menjadi -COO⁻.
Struktur Protein dan Perbandingan dengan Senyawa Amfoter Lain, Protein bersifat amfoter: bereaksi dengan asam dan basa
Sifat amfoter protein berasal dari gugus-gugus fungsionalnya yang dapat terionisasi. Pada pH rendah (asam), gugus -NH₂ akan menerima proton (H⁺) dan bermuatan positif, sedangkan pada pH tinggi (basa), gugus -COOH akan melepas proton dan bermuatan negatif. Perilaku ini mirip dengan senyawa amfoter lain seperti aluminium hidroksida (Al(OH)₃), yang dapat bereaksi dengan asam dan basa kuat. Namun, perbedaannya terletak pada kompleksitas; protein memiliki banyak gugus yang dapat terionisasi dengan nilai pKa yang berbeda, sehingga perilakunya lebih dinamis dan bergantung pada pH lingkungan.
| Senyawa | Perilaku sebagai Asam | Perilaku sebagai Basa | Sifat |
|---|---|---|---|
| HCl | Melepas H⁺ | Tidak berlaku | Asam kuat |
| NaOH | Tidak berlaku | Menerima H⁺ | Basa kuat |
| Al(OH)₃ | Al(OH)₃ + OH⁻ → Al(OH)₄⁻ | Al(OH)₃ + 3H⁺ → Al³⁺ + 3H₂O | Amfoter |
| Protein | R-COOH → R-COO⁻ + H⁺ | R-NH₂ + H⁺ → R-NH₃⁺ | Amfoter |
Reaksi Kimia Protein dengan Asam dan Basa
Reaksi antara protein dengan asam dan basa bukanlah konsep abstrak, tetapi proses kimiawi yang dapat diamati dan diprediksi. Reaksi ini melibatkan transfer proton antara gugus fungsional protein dan ion-ion dari larutan. Proses ini mengubah muatan keseluruhan molekul protein, yang pada akhirnya memengaruhi kelarutan, stabilitas, dan fungsinya.
Mekanisme Reaksi dan Pembentukan Garam
Ketika protein direaksikan dengan asam kuat seperti HCl, ion H⁺ dari asam akan disumbangkan kepada gugus amina yang bersifat basa pada rantai samping asam amino (seperti lisin atau arginin), membentuk gugus amonium yang bermuatan positif (R-NH₃⁺). Sebaliknya, ketika bereaksi dengan basa kuat seperti NaOH, ion OH⁻ akan bereaksi dengan proton dari gugus karboksilat (misalnya pada asam aspartat atau glutamat), menyebabkan gugus tersebut melepas proton dan berubah menjadi karboksilat bermuatan negatif (R-COO⁻).
Perubahan muatan ini bersifat reversibel dan sangat bergantung pada pH.
Menggunakan glisin, asam amino paling sederhana, sebagai model, kita dapat menulis persamaan reaksi setaranya.
Reaksi dengan HCl (Asam): H₂N-CH₂-COOH + HCl → ⁺H₃N-CH₂-COOH + Cl⁻
Reaksi dengan NaOH (Basa): H₂N-CH₂-COOH + NaOH → H₂N-CH₂-COO⁻ Na⁺ + H₂O
Perhatikan bahwa pada reaksi dengan basa, produk yang dihasilkan adalah sodium glycinate, suatu garam. Ini adalah inti dari bagaimana sifat amfoter bekerja; protein membentuk garam ketika bereaksi dengan asam atau basa kuat. Reaksi dengan asam menghasilkan garam ammonium, sedangkan reaksi dengan basa menghasilkan garam karboksilat.
Titik Isoelektrik dan Implikasinya
Konsep titik isoelektrik (pI) merupakan konsekuensi langsung dan paling penting dari sifat amfoter protein. Titik isoelektrik didefinisikan sebagai nilai pH spesifik dimana muatan positif dan negatif pada suatu molekul protein tepat saling meniadakan, sehingga muatan bersihnya menjadi nol. Pada titik ini, protein berada dalam keadaan zwitterion.
Nilai pI suatu protein ditentukan oleh komposisi asam aminonya. Protein yang kaya akan asam amino bermuatan basa, seperti lisin dan arginin, akan memiliki pI yang tinggi (basa), karena membutuhkan pH tinggi untuk menetralkan muatan positifnya. Sebaliknya, protein yang kaya asam amino asam, seperti asam aspartat dan glutamat, akan memiliki pI yang rendah (asam).
Pengaruh pH terhadap Kelarutan dan Aplikasi Praktis
Perilaku protein pada berbagai pH relatif terhadap pI-nya memiliki implikasi mendalam. Pada pH di bawah pI, lingkungan asam menyebabkan protein bermuatan positif secara keseluruhan. Pada pH di atas pI, lingkungan basa menyebabkan protein bermuatan negatif. Muatan ini menciptakan tolakan elektrostatik antar molekul protein dan menarik molekul air, sehingga protein mudah larut. Namun, pada pH = pI, muatan bersih nol menghilangkan tolakan antar molekul.
Protein akan cenderung berkumpul, mengalami agregasi, dan mengendap, sehingga kelarutannya mencapai titik terendah.
| Kondisi pH | Muatan Bersih Protein | Kelarutan | Kecenderungan |
|---|---|---|---|
| pH < pI | Positif | Tinggi | Tolakan antar molekul, larut |
| pH = pI | Nol | Sangat Rendah | Agregasi dan pengendapan |
| pH > pI | Negatif | Tinggi | Tolakan antar molekul, larut |
Pemahaman ini dimanfaatkan dalam pemurnian protein, seperti dalam proses isolasi protein whey atau enzim tertentu. Dengan menyesuaikan pH larutan campuran hingga sama dengan pI protein target, protein tersebut akan mengendap dan dapat dipisahkan dari protein lain dan kotoran yang masih larut.
Aplikasi dan Contoh Fenomena dalam Kehidupan Sehari-hari
Sifat amfoter protein bukan hanya teori laboratorium; ia adalah prinsip yang bekerja dalam tubuh kita dan berbagai produk yang kita gunakan sehari-hari. Dari proses pencernaan hingga pembuatan makanan, pemahaman tentang bagaimana protein berinteraksi dengan asam dan basa sangatlah penting.
Peran dalam Sistem Biologis dan Industri
Source: slidesharecdn.com
Dalam tubuh, protein darah, khususnya hemoglobin dan albumin, bertindak sebagai buffer (penyangga) biologis yang penting. Mereka membantu mempertahankan pH darah sekitar 7.4 dengan cara menerima ion H⁺ ketika lingkungan menjadi terlalu asam, atau melepasnya ketika lingkungan menjadi terlalu basa. Dalam industri farmasi, pengetahuan tentang pI digunakan untuk memformulasi obat protein seperti insulin, memastikan stabilitas dan kelarutannya yang optimal dalam sediaan obat.
Contoh klasik dalam industri pangan adalah pembuatan yogurt dan keju. Pembuatan yogurt melibatkan fermentasi laktosa dalam susu oleh bakteri menjadi asam laktat. Penurunan pH ini membawa protein susu (kasein) mendekati titik isoelelektriknya, menyebabkan protein menggumpal dan memadatkan susu menjadi yogurt. Pada pembuatan keju, enzim rennet ditambahkan untuk memotong rantai kasein secara spesifik, dan keasaman yang dikontrol memanfaatkan sifat amfoter untuk mengendapkan kasein menjadi dadih keju.
Di laboratorium medis, tes urine seringkali memeriksa protein. Prinsipnya adalah dengan memanipulasi pH; jika pH urine diatur ke titik isoelektrik protein, kehadiran protein akan terlihat sebagai kekeruhan atau endapan, yang mengindikasikan suatu kondisi medis seperti penyakit ginjal.
Eksperimen dan Demonstrasi Sederhana
Mendemonstrasikan sifat amfoter protein dapat dilakukan dengan mudah dan aman menggunakan bahan-bahan yang tersedia di rumah. Eksperimen ini memberikan bukti visual yang jelas tentang bagaimana protein merespons perubahan pH.
Prosedur Demonstrasi dengan Putih Telur
Eksperimen ini menggunakan putih telur (albumin) sebagai sumber protein. Albumin memiliki pI sekitar 4.7. Tujuannya adalah untuk mengamati kelarutan albumin pada berbagai pH.
Bahan dan alat yang diperlukan:
- Putih telur ayam mentah, diencerkan dengan air dengan perbandingan 1:1
- Larutan asam (cuka dapur / asam asetat encer)
- Larutan basa (larutan soda kue / natrium bikarbonat dalam air)
- Gelas kimia atau gelas bening (3 buah)
- Pipet tetes atau sendok kecil
- Pengaduk
Langkah-langkah percobaannya:
- Siapkan tiga gelas yang masing-masing berisi 50 mL larutan putih telur encer.
- Pada gelas pertama (kontrol), tidak ditambahkan apa-apa. Amati bahwa larutan tetap jernih atau sedikit keruh.
- Pada gelas kedua, tambahkan cuka tetes demi tetes sambil diaduk. Amati bahwa larutan tetap jernih atau bahkan menjadi lebih jernih karena asam melarutkan protein (pH jauh di bawah pI, muatan positif).
- Pada gelas ketiga, tambahkan larutan soda kue tetes demi tetes. Akan terbentuk gumpalan-gumpalan putih atau endapan. Ini terjadi karena penaikan pH mendekati pI albumin (sekitar 4.7), sehingga protein mengendap.
- Sebagian percobaan, coba tambahkan cuka ke dalam gelas ketiga yang telah mengendap. Endapan akan larut kembali karena pH diturunkan jauh di bawah pI.
Konsep keamanan yang perlu diperhatikan adalah menggunakan apron dan kacamata pelindung jika tersedia, hindari kontak dengan mata, dan jangan mencicipi bahan yang digunakan. Cuci tangan setelah percobaan.
Simpulan Akhir: Protein Bersifat Amfoter: Bereaksi Dengan Asam Dan Basa
Menguasai konsep protein bersifat amfoter membuka pintu untuk memanipulasi dan memanfaatkan molekul-molekul ini dengan presisi, baik di laboratorium penelitian, industri pangan, maupun dalam memahami fisiologi tubuh. Ini adalah pengingat yang kuat bahwa dalam dunia biokimia, konteks adalah segalanya—sedikit perubahan keasaman dapat mengubah seluruh nasib dan fungsi sebuah protein. Dengan pengetahuan ini, kita tidak hanya menjadi pengamat tetapi juga perancang yang dapat memprediksi dan mengendalikan interaksi molekuler yang mendukung kehidupan dan inovasi.
Informasi FAQ
Apakah semua protein memiliki sifat amfoter?
Ya, pada tingkat dasar, semua protein memiliki sifat amfoter karena semuanya tersusun dari asam amino yang mengandung gugus amino dan karboksil. Namun, kekuatan dan titik isoelektriknya sangat bervariasi tergantung pada komposisi dan urutan asam aminonya.
Mengapa yogurt tidak larut kembali ketika dinetralkan setelah diasamkan?
Pengasaman susu menyebabkan denaturasi dan penggumpalan protein yang tidak dapat balik. Meskipun pH dapat dinetralkan, struktur protein tiga dimensi yang telah berubah dan ikatan yang terbentuk antar molekul protein tidak dapat kembali ke bentuk aslinya, sehingga tekstur padat yogurt tetap bertahan.
Bisakah sifat amfoter protein menyebabkan masalah dalam tubuh?
Dalam kondisi normal, tubuh mengatur pH dengan ketat. Namun, penyakit tertentu yang menyebabkan pH darah menjadi sangat asam atau basa (asidosis/alkalosis) dapat mengganggu muatan dan fungsi protein, yang berpotensi mengganggu proses seluler vital.
Apakah sifat amfoter hanya dimiliki oleh protein?
Tidak, senyawa lain seperti aluminium hidroksida (Al(OH)₃) juga bersifat amfoter. Namun, protein adalah contoh kompleks dari senyawa amfoter polimerik dengan fungsi biologis yang sangat beragam.